Ficatul de șoc, sau numit și insuficiență hepatică acută, este apariția unor complicații severe la scurt timp după primele semne ale bolii hepatice (cum ar fi icterul) și indică faptul că ficatul a suferit leziuni severe (pierderea funcției a 80-90% din celulele hepatice ). Complicațiile complexe sunt encefalopatia hepatică și afectarea sintezei proteinelor. Insuficiența hepatică acută afectează adesea tinerii și aduce o mortalitate foarte mare.
Insuficiența hepatică acută este un termen larg care include atât insuficiența hepatică fulminantă, cât și insuficiența hepatică subiectivă (sau debutul tardiv al insuficienței hepatice). Insuficiența hepatică fulminantă este frecvent utilizată pentru a descrie dezvoltarea encefalopatiei în decurs de 8 săptămâni de la apariția simptomelor la un pacient cu un ficat anterior sănătos. Insuficiența hepatică subiectivă este menținută la pacienții cu afecțiuni hepatice până la 26 de săptămâni înainte de apariția encefalopatiei hepatice.
Cauzele frecvente ale ficat de soc sunt supradozaj cu paracetamol (acetaminofen), reacție idiosincrazică la medicamente, consum excesiv de alcool (hepatită alcoolică severă), hepatită virală (hepatita A sau B - extrem de frecventă în hepatita C), ficat gras acut în timpul sarcinii și ficat gras idiopatic fără niciun motiv aparent) . Boala Wilson (acumularea ereditară de miere) se poate manifesta adesea în insuficiență hepatică acută.
Dezvoltarea edemului cerebral este principala cauză de morbiditate și mortalitate la pacienții cu insuficiență hepatică acută. Etiologia acestei hipertensiuni intracraniene nu este pe deplin înțeleasă, dar este considerată multifactorială. Pe scurt, hiperamonemia poate fi implicată în dezvoltarea edemului cerebral. Se crede că edemul cerebral este atât citotoxic, cât și vasogenic.
Edemul citotoxic este o consecință a osmoregulării celulare afectate în creier, ducând la edem astrocit. Umflarea astrocitelor corticale este cea mai frecventă observație în studiile neuropatologice ale edemului cerebral în ficatul de șoc.
În creier, amoniacul este detoxificat la glutamină prin amidarea glutamatului de către glutamina sintetază. Acumularea de glutamină în astrocite duce la umflarea astrocitelor și edem cerebral. Există dovezi clare ale nivelurilor crescute de glutamină în creier la modelele animale cu insuficiență hepatică acută. Legătura dintre nivelurile ridicate de amoniac și glutamină și creșterea hipertensiunii intracraniene a fost raportată la om.
Creșterea volumului de sânge intracranian și a fluxului sanguin cerebral este un factor în insuficiența hepatică acută. Creșterea fluxului sanguin cerebral se datorează afectării autoreglării cerebrale. Se consideră că perturbarea autoreglării cerebrale este mediată de concentrații sistemice crescute de oxid nitric, care acționează ca un vasodilatator puternic.
O altă consecință a insuficienței hepatice fulminante este insuficiența organelor în mai multe etape, care este adesea observată în contextul unei afecțiuni circulatorii hiperdinamice care imită sepsisul (rezistență vasculară sistemică scăzută). Prin urmare, insuficiența circulatorie și perfuzia slabă a organelor pot iniția sau contribui la complicații ale insuficienței hepatice fulminante.
Dezvoltarea insuficienței hepatice este rezultatul general final al unei largi varietăți de cauze potențiale, așa cum sugerează diagnosticul diferențial larg. La fel ca în cazul multor medicamente care suferă metabolism hepatic (în acest caz citocromul P-450), metabolitul oxidativ al acetaminofenului este mai toxic decât cel al medicamentului. Metabolitul activ extrem de reactiv N-acetil-p-benzoquinona-imină pare să medieze o mare parte din deteriorarea legată de acetaminofen a țesutului hepatic prin formarea de legături covalente cu proteinele celulare.
Al doilea scenariu și mai puțin evident apare la un pacient care consumă alcool în mod regulat. Acest lucru nu necesită neapărat un istoric de abuz de alcool sau alcoolism. Chiar și un băutor moderat sau social care consumă în mod regulat una până la două băuturi pe zi poate epuiza suficiente rezerve interne de glutation. Aceasta are ca rezultat o hepatotoxicitate potențial letală din ceea ce altfel este o doză sigură de acetaminofen (sub doza maximă totală de 4 grame/decilitru) la o persoană nebănuită. Pacienții cu ficat de soc poate avea o toxicitate neregulată sau incertă a acetaminofenului.
Descoperirile biopsiei hepatice pot fi nespecifice, dar în general rezultatele depind de etiologia subiacentă a ficatului de șoc.
Probele de biopsie hepatică la pacienții cu hepatită idiosincrazică indusă de medicamente care duc la insuficiență hepatică fulminantă prezintă de obicei necroză patoglobulară. Necroza centroblobulară este caracteristică pacienților cu insuficiență hepatică fulminantă cauzată de acetaminofen, dar pot apărea și traume patoglobulare.
Hepatita virală cauzează de obicei leziuni patoglobulare și poate fi dificil de distins de hepatita indusă de medicamente. Prezența steatozei microvesiculare sugerează unele medicamente (de exemplu, acidul valproic, salicilații în sindromul Reye) ca cauză a insuficienței hepatice fulminante, dar această constatare este observată și în ficatul gras acut în timpul sarcinii.
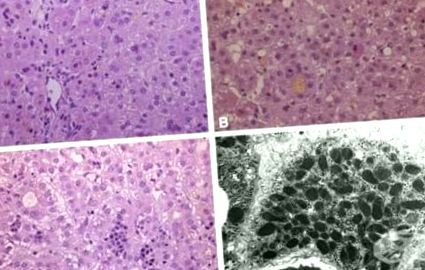
Caracteristică este dispariția glicogenului și apariția așa-numitelor celule strălucitoare Kraevsky. În plus, în funcție de severitatea șocului, există necroză a hepatocitelor individuale sau necroză hepatică centrolobulară. Sinusoidele conțin multe leucocite neutrofile și microtrombi cu fibrină unică. Spațiile Disse sunt edematoase. Celulele Kupffer sunt umflate și produsele de degradare a fibrinei fagice sunt detectate în ele.
- Hemangiom al ficatului Patologie
- Tumori hepatice Patologie
- Hemangiom hepatic BG-Mamma
- Pachet CEAI FICAT 70 g
- Simptom mărit al ficatului și splinei