O caracteristică comună a revărsărilor pleurale inflamatorii (PI) este procesul inflamator al foilor pleurale. Majoritatea pleureziei apare în procesele inflamatorii purulente ale structurilor adiacente (pneumonie, mediastinită, abces, abces hepatic, abces subdiafragmatic, paranefrită, pancreatită etc.), precum și în organe și sisteme mai îndepărtate (osteomielită, otită și altele .). IP-urile inflamatorii sunt exudate în natură. Cele mai frecvente cauze ale exsudatelor pleurale sunt prezentate în tabel. 1.
Tabelul 1. Cauzele revărsărilor pleurale exudative.
Revărsături pleurale inflamatorii infecțioase
În țările dezvoltate, infecțiile sunt a doua cauză cea mai frecventă (după insuficiența cardiacă) a PI. Infecțiile pleurale provoacă de obicei revărsări exudative. Cele mai frecvente dintre acestea sunt revărsările pleurale parapneumonice; se estimează că cel puțin 40% dintre pacienții cu pneumonie dezvoltă PI. Răspunsul inflamator duce la creșterea permeabilității capilare cu pierderea de proteine prin patul capilar. În același timp, datorită depunerii de fibrină și îngroșării inflamatorii a membranei pleurale, reabsorbția fluidelor și proteinelor prin vasele limfatice este afectată. Cei mai comuni agenți infecțioși ai pleureziei sunt bacteriile. Ciupercile, virusurile și paraziții sunt cauze destul de rare ale reacțiilor inflamatorii pleurale.
Revărsături pleurale bacteriene parapneumonice. Un revărsat asociat cu faza acută a pneumoniei (bacteriană sau virală) este denumit în general parapneumonic și este cea mai frecventă cauză de pleurezie exudativă. Se clasifică în trei categorii (grade): (1) necomplicat (revărsat liber, mic, neinfectat, resorbabil după antibioterapie); (2) complicat (infectat cu un agent infecțios, adesea încapsulat, care necesită drenaj pleural) și (3) empiem (acumularea de puroi în cavitatea pleurală în terapia inadecvată a revărsării complicate și ca stadiu final al acestuia).
Potrivit lui R. Light și colab. (2006) PI în abcesul pulmonar este denumit și parapneumonic 2 .
Ponderea PI parapneumonic conform N. Paleev și colab. este 18-70% din toate revărsările. Potrivit lui R. Fraser și colab. și A. Fein și colab. astfel de revărsări sunt observate în 40% din cazurile de pneumonie și conform lui G. Baum și colab. - în 36-57%. Ele variază în severitate în intervalul dintre revărsările necomplicate și empiemul pleural. La 10% dintre aceștia sunt necesare toracostomie și drenaj, mai ales în caz de empiem sau revărsat încapsulat. Acest procent, desigur, este mult mai mare, deoarece revărsatul este adesea mic și imperceptibil din punct de vedere radiologic. Frecvența ar fi mai mare dacă laterografia ar fi efectuată în toate cazurile.
Potrivit lui R. Light și colab. PI este diagnosticată la 20 până la 40% din pneumoniile bacteriene, proporția revărsărilor parapneumonice în pneumonie cauzate de Klebsiella pneumoniae fiind de 10%, iar la Streptococcus pyogenes și Staphylococcus aureus ajungând la 70-95%. Pneumonia Haemophylus influenzae este însoțită de PI în 50% din cazuri. Același este procentul de revărsări în pneumonia stafilococică. Potrivit lui R. Light, prezența PI parapneumonică crește probabilitatea unui rezultat fatal în pneumonie 1.2 .
În revărsările necomplicate care apar în primele 48-72 de ore (imediat după etapa scurtă „uscată”), se formează un exudat de volum mic, galben pai, transparent, steril, care este absorbit în paralel cu resorbția infiltratului pneumonic . Cel mai adesea, neutrofilele peste 10.000/ml predomină în lichidul pleural. Rareori, revărsatul este tulbure sau purulent. PH-ul pleural este în general> 7,20-7,30, glucoza pleurală este> 3,3 mmol/l (> 60 mg/dl [R. Light, 2006]), iar LDH este 2 .
Dacă inflamația persistă, deteriorarea endotelială continuă și atunci cantitatea de revărsat crește. Crește și probabilitatea de invazie și persistență a microorganismelor în cavitatea pleurală. Se dezvoltă PI complicată, care cu un tratament antibiotic inadecvat poate apărea rapid (în câteva ore).
Cel mai important punct în PI parapneumonic nu este acela de a-și dovedi natura exudativă sau transudativă. Este mai important să se diferențieze acele cazuri care pot evolua spre revărsări complicate, care în dezvoltarea exsudaților parapneumonici sunt o etapă de tranziție către empiem. Persistența neutrofiliei pleurale, liza celulară ulterioară, creșterea suplimentară a LDH pleural (adesea peste 1000 UI/l) sau de trei ori peste norma serică superioară (R. Light, 2006), scăderea nivelului de glucoză 2. Culturile microbiologice în acest stadiu pot fi, de asemenea, negative datorită eradicării rapide inițiale a bacteriilor.
Odată cu dezvoltarea empiemului în cavitatea pleurală, se acumulează puroi și se înregistrează clinic febra și leucocitoza. Acest lucru se întâmplă cu o contaminare bacteriană persistentă a revărsatului, ducând la o creștere a numărului de neutrofile. Lichidul pleural capătă un aspect purulent cu acidoză a exudatului (pH pleural 7,1-7,3) datorită metabolismului anaerob al glucozei PMN și al bacteriilor. Ca produs final al metabolismului glucozei, CO2 și acidul lactic se acumulează în cavitatea pleurală cu o scădere ulterioară a pH-ului sub 7,1. Nivelul pH-ului PI este considerat a fi cel mai sensibil indicator biochimic al empiemului de revărsare, deoarece scade mai repede decât nivelul glucozei. Fagocitoza neutrofilă și metabolismul bacterian scad, de asemenea, nivelul glucozei pleurale (glicoliză). Pe măsură ce debitul devine mai complicat, valoarea acestuia din urmă scade sub 2,2 mmol/l. Cu alte cuvinte, cu cât glucoza și pH-ul din lichidul pleural sunt mai mici, cu atât este mai probabilă natura bacteriană a inflamației. Datorită lizei celulare în faza PI complicată, crește valoarea LDH pleurală, care ajunge la peste 1000 UI/l.
Dacă cavitatea pleurală nu este drenată, lichidul devine din ce în ce mai localizat, formarea buzunarelor pleurale devine mai palpabilă, iar PI intră în faza clinică finală (a treia etapă conform R. Light, 2006) a PI parapneumonic complicat, cu care se termină.asa-numitul stadiul fibropurulent - stadiul de organizare (fibroză). Intrarea fibroblastelor metabolice active în cavitatea pleurală duce la formarea de cheaguri de fibrină, membrane și depozite de fibrină pe suprafețele pleurale, secreția glucozaminoglicanilor și a colagenului, formarea fibrelor de fibrină, punțile țesuturilor și articulațiile pleurale groase, inelastice. Asa numitul empiem organizat (plămân prins) în care este dificil să se extindă plămânii atunci când respirați. Este necesară formarea ulterioară a fistulei bronho-pleurale, a abcesului pulmonar sau a empiemului (perforație spontană prin peretele toracic) 1, 2 .
În empiemul pleural, culturile microbiologice sunt de obicei pozitive. Valoarea pH-ului pleural este unul dintre cele mai utilizate teste clinice pentru a determina revărsările cu tendință de drenaj pleural (vezi Tabelul 2). Se consideră că valoarea pH-ului sub 7,2 este pragul de pornire a drenajului, iar la pH sub 7,1 ar trebui să se facă de urgență. Cu toate acestea, trebuie avut în vedere că revărsările de malignitate, artrita reumatoidă, tuberculoza, lupusul sistemic și uremia pot apărea și cu pH pleural scăzut. Orice revărsat cu o pată Gram pozitivă este indicat și pentru drenaj. Toate indicațiile moderne pentru drenajul pleural în revărsările pleurale parapneumonice sunt prezentate în tabel. 2 și în tabel. 3 prezintă factorii asociați cu un prognostic slab al PI parapneumonică.
Cursul clinic al revărsărilor pleurale parapneumonice bacteriene 1,2 .
În majoritatea cazurilor, cursul clinic se suprapune cu cel al pneumoniei. Debutul este acut, cu temperatură corporală ridicată (până la 39 ° C), oboseală severă, transpirație, tuse, adesea cu expectorație și la un procent mic de pacienți cu hemoptizie (până la 4%). La unii pacienți există dureri toracice la respirație, iar la unii dintre ei există dificultăți de respirație în repaus (30-40%). Mai des decât în alte pleurezi, se înregistrează leucocitoză și VSH accelerată peste 50 mm. Leucocituria, proteinuria și eritrocituria pot fi înregistrate în urină. Prezența infecției pulmonare anaerobe se caracterizează printr-o tendință de evoluție cronică, anemie și scădere în greutate.
Tabelul 2. Factori de prognostic pentru drenajul pleural sau alte proceduri invazive în revărsările pleurale parapneumonice (conform lui D. Bouros, H. Hamm).
Aceasta este una dintre cele mai vechi și mai grave boli pleurale, despre care Hipocrate a scris: „Dacă empiemul nu izbucnește, apare moartea”. În fiecare an, în Statele Unite și Marea Britanie, empiemul și IP complicate afectează 65.000 de pacienți, rezultând costuri financiare uriașe (500 de milioane de dolari) și mortalitate de 20%. Zonele preferențiale pentru dezvoltarea sa sunt zonele paravertebrale posterioare și laterale ale cavității pleurale. Colorarea Gram poate să nu prezinte un rezultat pozitiv din cauza infecției frecvente cu anaerobi, care sunt dificil de izolat și identificat. Situația este similară la pacienții care au fost deja tratați cu antibiotice. Pacienții imunocompromiși și pacienții care primesc terapie cu glucocorticosteroizi pot avea temperatura corporală normală și un număr normal de leucocite din sânge. Empiemul netratat este rar resorbit spontan. Se poate scurge prin peretele toracic (necesită empiemul) sau în plămâni (cu fistulă bronho-pleurală).
Depistarea precoce a pacienților cu tendința de a complica PI parapneumonic ajută la efectuarea drenajului pleural precoce, care (indiferent de terapia antimicrobiană adecvată) previne septarea fibrinoasă, încapsularea și dezvoltarea sepsisului. Din păcate, distincția necomplicată de PI complicată devine dificilă din motive clinice, dar numai cu analiza lichidului pleural. Nivelul proteinei pleurale, compoziția celulară sau numărul de neutrofile sunt irelevante. Analiza biochimică are cea mai mare valoare: dacă pH-ul este sub 7,1, glucoza
- sub 2,2 mmol/l și LDH - peste 1000 UI/l, revărsatul este complicat și necesită drenaj pleural. Dacă puroiul este înregistrat în timpul toracentezei, drenajul nu poate fi întârziat. Cu toate acestea, dacă pH-ul este peste 7,30, glucoza - peste 3,3 mmol/l și LDH
- sub 1000 UI/l, revărsatul este necomplicat și este de obicei resorbit sub influența unei chimioterapii antimicrobiene adecvate. Prezența empiemului fără infiltrat pneumonic poate fi o expresie a așa-numitului empiem postpneumonic, în care pneumonia a fost deja resorbită.
Spectrul microbiologic al empiemului pleural
În țările occidentale, datorită unui control bun al tuberculozei și a bunei terapii cu antibiotice, majoritatea empiemelor bacteriene sunt cauzate nu de Streptococcus pneumoniae, ci de Staphylococcus aureus, bacili enter negativi Gram și anaerobi. Culturile prezintă cel mai adesea o floră mixtă de bacterii aerobe și anaerobe, iar bacteriile Gram-negative predomină la pacienții spitalizați cu empiem. Cele mai frecvente cauze ale empiemului sunt prezentate pe
Tabelul 4. Cele mai frecvente cauze ale empiemului pleural (conform lui A. Fein și colab.) 3 .
| № | Microorganisme | Frecvență (%) |
| 1. | Anaerobi | 30-70 |
| 2. | Staphylococcus aureus | 25-35 |
| 3. | Bacili gram negativi | 20-30 |
| 4. | Streptococcus pneumoniae | 5-15 |
| 5. | Culturi negative | 3-30 |
| 6. | Flora polimicrobiană | 30-70 |
Majoritatea pneumoniilor la pacienții adulți spitalizați ale căror sisteme imune sunt compromise prin medicație sau intervenții chirurgicale sunt cauzate de grupul Klebsiella-Enterobacter-Serratia; aceste pneumonii sunt prea des complicate de empiem. Pneumonia cauzată de Klebsiella tip I, III, IV și V se dezvoltă la alcoolici sau pacienți cu dizabilități severe, este rareori nosocomială și de obicei prezintă PI complicată. Empyema este adesea o complicație a pneumoniei cauzate de respectivul grup de microorganisme, împreună cu Escherichia coli și Pseudomonas aeruginosa. În majoritatea cazurilor de Pseudomonas aeruginosa-pneumonie, este detectată o revărsare purulentă nedetectată cu autopsie. Agenții anaerobi sunt izolați în culturile de lichide pleurale în 6% până la 38% din cazuri. Empiemele anaerobe au un miros prost (putrid).
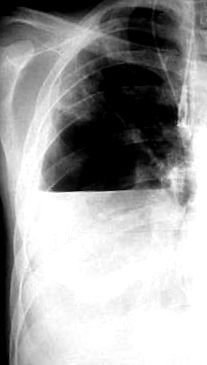
Nu există criterii radiologice în literatură care să indice un agent etiologic specific, dar există două excepții de la această regulă: o infecție cauzată de Clostridium perfringens și Bacteroides fragilis are caracteristici radiologice specifice. Aceste bacterii duc la formarea gazului în țesuturile moi ale peretelui toracic și în cavitatea pleurală, care pot forma imaginea piopneumotoraxului (vezi Fig. 1).
Figura 1. Raze X cu piopneumotorax drept la un pacient cu leiomiom și perforație a esofagului (D. Kostov) 1
Alte cauze ale empiemului pleural
Pe lângă infecțiile pulmonare (pneumonie bacteriană), în empiem pot fi luate în considerare și alte cauze etiologice. Majoritatea empiemelor neumonice sunt iatrogene, cel mai adesea complicații ale intervenției chirurgicale (vezi Tabelul 5). Chirurgia toracică este responsabilă pentru aproximativ 20% din toate empiemele. Aproximativ 5-6% apar după un traumatism toracic sau o perforație esofagiană (adesea iatrogenă). Toracocenteza sau pneumotoraxul spontan sunt responsabile pentru 2% din cazuri, iar aproximativ 1% se datorează infecțiilor abdominale (după colecistectomie sau splenectomie).
Tabelul 5. Cauze ale empiemului pleural (conform lui D. Bouros, H. Hamm) 4 .
- Boli inflamatorii ale articulațiilor - fizioterapia ajută
- Alimente sănătoase pentru boli inflamatorii cronice intestinale
- Prăjituri de casă
- Despre brânza galbenă bulgară și secretul producției sale
- Banda de alergare FALCON Banda de alergare B2 la preț TOP în Sofia, Bulgaria, în rate