Prof. Dr. Georgi Mihailov, dr. Victoria Varbanova
Spitalul specializat pentru tratamentul activ al bolilor hematologice (SBALHZ), Sofia
Anemia este un grup eterogen de boli caracterizate prin scăderea concentrației de hemoglobină (Hb), hematocrit (Hct) sau număr de eritrocite (RBC) sub normal: Hb [1-3]. Aproximativ 30 până la 70% din populația din țările în curs de dezvoltare are deficit de fier, cu cea mai mare incidență în rândul persoanelor care urmează o dietă săracă în fier sau la pacienții cu sângerări gastrointestinale cronice [1,2,4]. Toate femeile însărcinate, adolescenții și sugarii prematuri prezintă, de asemenea, un risc crescut.
Fierul este un nutrient esențial necesar pentru dezvoltarea normală a fiecărei celule umane. Funcția sa principală în organism este determinată de participarea sa la sinteza hemoglobinei (70%) și mioglobinei (10%), adică. ca transportator de oxigen către fiecare celulă. În plus, fierul servește ca mediator al schimbului enzimatic de electroni (citocromi, peroxidaze, ribonucleotid reductază și catalază, în total 20%).
Etiologie și patogenie: Există numeroase clasificări ale JDA. Clasificarea pe baza criteriilor etiologice și patogenetice este cea mai aplicabilă în practica clinică (Tabelul 1):
І Nevoi crescute de Fe
- Anemii post-hemoragice acute și cronice.
- JDA pentru nevoile crescute de Fe - nou-născuți, adolescenți, sarcină și alăptare.
II Importuri insuficiente de Fe
- JDA nutrițional.
- JDA resorptiv.
- Transportul afectat al Fe.
III JDA în alte boli (IDA secundar, boli infecțioase, inflamatorii sistemice, boli neoplazice).
Nevoi crescute de Fe
Aport insuficient de Fe
1. Deficitul alimentar de Fe biodisponibil
2. Absorbția afectată a Fe
Rezecția gastrică
2. Donarea de sânge
3. Transportul afectat al Fe
3. Tratamentul anemiei cu deficit de vitamina B12
5. Sarcina și alăptarea
Masa. 1. Etiologia JDA.
Tablou clinic:
- Simptomele asociate cu sindromul anemic: asteno-adinamia, pielea palidă și membranele mucoase, dispneea de efort, suflul inimii sistolice.
- Modificări mucocutane: cuie concavă (koilonyhia) [17], păr și unghii fragile, piele uscată, sindromul Plumer-Vinson sau Paterson-Kelly (atrofie sideropenică a căptușelii limbii, orofaringe și esofag cu arsuri ale limbii și disfagie dureroasă) [18 unghiular cheilită.
- Simptome neurologice: Sindromul Ekbom - o tulburare neurologică caracterizată prin mișcări involuntare sau ticuri ale extremităților inferioare (acatisie) [19] .
- Alții: hemoragii/exudate de retină (rare, deficit de Fe cronice), splenomegalie (rare, deficit de Fe cronice).
Cercetări de laborator
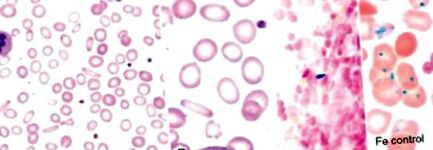
PAC: anizocitoza și creșterea RDW (lățimea de distribuție a eritrocitelor) este un semn morfologic precoce, dar nu obligatoriu (Fig. 1), ovalocite, celule țintă. Hipocromie progresivă (valori scăzute ale MCHC) și microcitoză (valori scăzute ale MCV). Leucopenia este observată la un procent scăzut de pacienți cu DCC normal. Trombocitopenie - la ¼ la copii și adolescenți, dar nu tipică la adulți. S-a raportat cromocitoză la 1/3 din pacienții cu deficit de JDA la copii, în timp ce la adulți se găsește în cazuri rare, în principal în boli neoplazice concomitente sau infecții cronice. Reticulocite: număr scăzut sau normal.
FIG. 1. Modificări morfologice în JDA: PKK: eritrocite microcitice hipocrome cu anulocite și anizocitoză, granulocite hipersegmentate (A), (B). Colorarea albastră prusiană a unui aspirat de măduvă osoasă a arătat o reducere semnificativă a depozitelor de Fe în măduva osoasă (C).
Feritină plasmatică este cel mai fiabil indicator indirect pentru măsurarea depozitelor de fier. Valorile feritinei plasmatice sub 12 mg/L sunt patognomonice pentru epuizarea depozitelor de Fe. În DD, singurele cauze ale scăderii feritinei plasmatice care nu sunt asociate cu JDA sunt hipotiroidismul și deficitul de Vit B6 [20]. În schimb, în bolile inflamatorii (infecții acute, poliartrită reumatoidă, boli inflamatorii cronice), concentrația serică de feritină, ca proteină în fază acută, crește ca urmare a creșterii producției (Tabelul 2, Tabelul 3). O creștere similară se observă în citoliza organelor parenchimatoase bogate în feritină.
Transferrin (β1-globulina) este o proteină de transport majoră a Fe în sânge și capacitatea sa de legare a fierului (= JSC total) se schimbă invers cu concentrația serului Fe.
Concentrația plasmatică a receptorului de transferină solubil este o nouă metodă fiabilă pentru determinarea deficitului de fier tisular. Receptorul transferrin solubil este un derivat al receptorului transferinei tisulare cu o greutate moleculară de 85.000 D. Un procent mai mare de receptori ai transferinei plasmatice provin din eritonul din măduva osoasă și concentrația lor este direct dependentă de activitatea precursorului eritroidian în os măduvă. Concentrațiile plasmatice scăzute ale receptorilor solubili ai transferinei sunt caracteristice hipoplaziei eritroide (anemie aplastică, insuficiență renală cronică, deficit de fier), în timp ce concentrațiile crescute se observă în hiperplazia eritroidă (talasemie, anemie falciformă, anemie, anemie disemică și dislită). În timp ce concentrația plasmatică a feritinei poate fi crescută în mod disproporționat în raport cu depozitele de fier din organism, în bolile inflamatorii concomitente sau bolile hepatice, concentrația plasmatică a receptorului de transferină solubil nu este afectată și este un indicator de laborator mai fiabil al deficitului de fier [20] . Metodele imunologice pentru determinarea nivelurilor plasmatice ale receptorilor de transferină solubile intră deja în practica clinică [21] .
Biopsia măduvei osoase este indicat la un număr mic de pacienți pentru DD de DDA pentru a demonstra depleția depozitelor de Fe în măduva osoasă și numărul redus de sideroblaste.
Etapele deficitului de fier (Fig. 2)
Deficitul de fier prelat: stadiul deficitului de Fe în depozitele de deșeuri.
Deficiență latentă de fier: stadiul eritropoiezei cu deficit de fier fără anemie, adică. se reduce concentrația de Fe în măduva osoasă și ser.
Anemie manifestă: se manifestă ca JDA.
FIG. 2. Etapele deficitului de Fe.
Diagnosticul diferențial (DD) - Masa. 2 și Tabel. 3.
Și talasemia și hemoglobiopatia
II Tulburări în sinteza hemoglobinei datorită utilizării substanțelor chimice și a medicamentelor
III Altele
Anemie în inflamația cronică
Masa. 2. DD cu alte anemii microcitice care nu sunt cauzate de deficit de Fe
ЖДА
JDA secundar la nivel inflamatorși boli neoplazice
Talasemie
Mielodisplazie
Fe seric
SA total
Ferritin
Receptor de transferină solubil
Măduva spinării
lipsa rezervelor de Fe
Fe în macrofage
suficiente stocuri de Fe
rezerve crescute de Fe, sideroblaste inelare
Masa. 3. DD de laborator al JDA cu alte anemii hipocrome [adaptat în 3]
Terapie
- Tratament etiologic.
- Terapia de substituție - se efectuează cu medicamente care conțin diferite săruri de Fe pentru administrare orală sau parenterală.
2.1 Terapia de substituție orală este considerată o metodă mai fiziologică de introducere a Fe, care este în formă bivalentă și este ușor de absorbit. Contraindicațiile relative sunt boala activă a ulcerului peptic, antecedente de melenă, gastrită atrofică cronică, hernie hiatică, gastrectomie, anastomoze gastro-intestinale.
Datorită capacității limitate de absorbție și transport, doza zilnică la adulți este cuprinsă între 150 și 200 mg de Fe elementar, împărțită în 3 sau 4 doze pe zi, cu o oră înainte de mese. La copii, doza pentru tratamentul activ este de
50-100 mg (3 mg fier elementar/kg greutate corporală) zilnic. Criteriul eficacității terapeutice este o creștere a Hb cu 2 g/dL după trei săptămâni de terapie, 1/2 din pacienți având o întârziere de 1-2 săptămâni. Pentru reaprovizionarea depozitelor de Fe, durata terapiei cu preparate orale de Fe este de cel puțin 12 luni după normalizarea nivelului de Hb sau până la o concentrație plasmatică de feritină ≥50 mg/L. Dacă cauza etiologică persistă, de ex. menometroragie se recomandă efectuarea tratamentului de întreținere și profilaxie în doze zilnice de 50-100 mg la adulți, respectiv 10-20 mg la copii.
În absența unui răspuns terapeutic în limitele de timp specificate, terapia de înlocuire cu preparate de Fe ar trebui întreruptă, având în vedere DD sindromul anemic și evaluarea posibilelor comorbidități: sindrom de malabsorbție, hemoragie necontrolată, Vit concomitent Deficit de B12 și/sau acid folic, boli inflamatorii cronice, boli infecțioase persistente, neoplazie, patologie hepatică, insuficiență renală.
Reacțiile adverse la medicament sunt rare (10-20%) și nu necesită de obicei întreruperea tratamentului. Reducerea dozei este discutată în cazul intoleranței gastro-intestinale severe (constipație, sindrom dispeptic superior sever, diaree, gust metalic în gură). Utilizarea concomitentă cu tetracicline, cloramfenicol și chinolone nu este recomandată datorită formării compușilor chelați și absorbției reduse, precum și cu antiacide sau inhibitori ai pompei de protoni.
Se utilizează în formele severe de JDA, în absorbția afectată a Fe (malabsorbție, gastrectomie, anastomoze gastro-intestinale), intoleranță la preparatele orale de Fe (colită, enterită), pacienți aflați în croniodializă (în paralel cu eritropoietina). Dacă se suspectează malabsorbția fierului, se recomandă screeningul prin administrarea a 100 mg de Fe elementar sub formă de sirop de sulfat de fier în post, urmat de măsurarea concentrațiilor plasmatice de Fe la 1 și 2 ore. La pacienții cu deficit de Fe și o concentrație inițială de Fe plasmatică mai mică de 50 mg/dL, este de așteptat în mod normal o creștere a Fe seric la 200-300 mg/dL. O creștere a Fe-ului plasmatic sub 100 mg/dL este suspectată de sindrom de malabsorbție și este o indicație pentru biopsia intestinului subțire.
Fe parenteral este în formă trivalentă și este stabilizat cu dextran sau zaharuri. Doza pentru tratamentul activ este individuală și se calculează în funcție de deficiența totală de fier conform formulei:
Total (ml) = deficit total de Fe (mg): 20 mg/ml
Deficiență totală de Fe (mg) = greutate (kg) x [niveluri de Hg dorite - nivel real de Hg (g/L) x 0,24 + depozit de Fe (mg)
Pacienți cu greutatea de până la 35 kg: depozit Fe = 15 mg/kg
Pacienți cu o greutate mai mare de 35 kg: depozit Fe = 500 mg
Reacțiile adverse din terapia cu medicamente parenterale sunt mai frecvente și sunt exprimate printr-o reacție anafilactică: alergii cutanate, bronhospasm la șoc anafilactic. O altă posibilă complicație secundară este manifestarea reacțiilor tardive asemănătoare bolii serice: febră, urticarie, adenopatie, mialgie și artralgie. Date SUA FDA pentru perioada 2001-2003 a raportat incidența reacțiilor adverse care pun viața în pericol de 11,3, 3,3, 0,9 și, respectiv, 0,6 la 1 milion, cu Fe-dextran cu greutate moleculară mică și cu complex de Fe-hidroxi zaharoză și zahăr Fe [23] .
Prognoza
Tratamentul etiologic și de înlocuire combinat al JDA duce la controlul sindromului anemic și la restabilirea capacității de lucru. Adesea, semne clinice și subiective de îmbunătățire constituțională sunt observate în primele câteva zile de tratament. Reticulocitoza moderată în unele cazuri severe de anemie cu deficit de Fe poate fi înregistrată la fiecare 3-5 zile, cu maxim 8-10 zile de terapie și o scădere treptată. Concentrațiile de Hb încep să crească după prima săptămână de terapie cu normalizarea valorilor timp de aproximativ 6 săptămâni. Recuperarea completă a microcitozei se observă cel mai adesea după a 4-a lună. Deși anomaliile mucoasei încep să se recupereze imediat odată cu începerea terapiei de substituție, dispariția glositei și a modificărilor unghiilor poate dura câteva luni. Lipsa unui răspuns terapeutic în termenele specificate ar trebui să ducă la o revizuire a diagnosticului și a DD cu alte anemii microcitice/hipocrome, precum și o evaluare a posibilelor comorbidități. Prognosticul la pacienții cu deficit de Fe depinde în principal de cauza etiologică.
Masa. 2. DD cu alte anemii microcitice care nu sunt cauzate de deficit de Fe
Masa. 1. Etiologia JDA.
- A MANCA IN ANEMIE
- Să mâncăm cu anemie
- Anemie cu deficit de fier
- Anemie cu deficit de fier - Cum se tratează (complicații) - Sănătate
- Anemie cu deficit de fier în timpul sarcinii