Un rezumat al noii strategii GINA: o foaie de parcurs către controlul astmului
Reddel H., Bateman E., Becker A. și colab.; Eur Respir J., 2015; 46 (3): 622-63
SABA Agoniști beta2 cu acțiune scurtă
ICS/LABA corticosteroizi inhalatori/agonist beta2 cu acțiune îndelungată
ICS corticosteroizi inhalatori
BPOC este o boală pulmonară obstructivă cronică
Astmul ACOS - sindromul BPD se suprapune
În ultimii 20 de ani, Inițiativa globală pentru astm (GINA) a publicat periodic o actualizare a Documentului global de comportament și prevenire a astmului, care stă la baza multor orientări naționale pentru tratamentul acestei boli. Cu toate acestea, noile orientări sunt slab implementate în practică. O revizuire majoră a fost publicată în 2014 și o actualizare ulterioară în 2015. Aceasta reflectă percepția astmului ca o boală eterogenă a căilor respiratorii, bazată pe o bază mai largă de dovezi, un interes crescând pentru o abordare terapeutică individuală și dovezi în favoarea unui astfel de comportament.
Articolul este un rezumat al modificărilor cheie din noul manual GINA, precum și justificarea acestora. Modificările includ o revizuire a definiției astmului; metode de evaluare a controlului simptomelor și factorilor de risc pentru apariția evenimentelor adverse; indicații extinse pentru terapia cu corticosteroizi inhalatori; cadrul pentru abordarea individuală a tratamentului bazat pe fenotip, factori de risc variabili, preferințele pacientului; optimizarea eficacității tratamentului prin verificarea tehnicii de inhalare și a aportului corect; realizarea unui plan scris pentru pacient cu privire la astm; diagnosticul și terapia inițială a astmului - sindrom de suprapunere a BPOC; strategii actualizate pentru adaptarea și implementarea recomandărilor GINA.
Astmul este o boală cronică gravă. Cu o frecvență cuprinsă între 1% - 20% în rândul adulților și peste 20% în rândul copiilor cu vârsta cuprinsă între 6 și 7 ani. Deși unele țări au înregistrat o scădere a mortalității legate de astm și a spitalizărilor în ultimii 20 de ani, exacerbările globale și simptomele de o zi au crescut cu aproape 30%. Impactul astmului este resimțit nu numai de pacienți, ci și de familiile acestora, de sistemul de sănătate și de societate. Astmul este una dintre bolile cronice frecvente care afectează copiii și tinerii. Există o creștere a frecvenței și a impactului asupra populației active.
Scopul al articolului este un rezumat al punctelor cheie din GINA cu o descriere a justificării pentru fiecare modificare. Noul raport încorporează o abordare inovatoare: orientată spre practică și bazată pe dovezi.
Capitolul 1: Ghiduri practice pentru diagnosticarea astmului
- Dezvoltarea unei noi definiții a astmului.
- Instrumente practice care conțin un tabel cu simptomele clinice caracteristice și testele de diagnostic. Recomandări pentru confirmarea diagnosticului la pacienții deja aflați în tratament, precum și pentru diagnosticarea bolii în grupuri specifice de pacienți, cum ar fi femeile însărcinate și adulții.
Modificările cheie sunt o consecință a noii definiții, care are ca scop reducerea atât a non-diagnosticului, cât și a supra-diagnosticului. Se pune accent pe punerea diagnosticului înainte de începerea tratamentului.
„Astmul este o boală eterogenă, caracterizată de obicei prin inflamația cronică a căilor respiratorii. Este determinată de prezența simptomelor pulmonare, precum: respirație șuierătoare, dificultăți de respirație, senzație de apăsare a pieptului și tuse, care se schimbă în timp, alături de o modificare a limitării dispneei expiratorii "[1]
"AstmEste folosit în mod intenționat ca termen general, cum ar fi „Anemie”, „Artrită”, „Carcinom”. Acest lucru facilitează comunicarea cu pacienții și recunoașterea acestei boli eterogene cu caracteristici clinice diferite.
Cuvântul „normal” din definiție îi îngrijorează pe unii cititori. Rațiunea este că, deși inflamația cronică a căilor respiratorii este o caracteristică majoră în cele mai cunoscute fenotipuri de astm, absența markerilor inflamatori nu ar trebui să excludă diagnosticul la pacienții cu simptome pulmonare variabile și limitarea fluxului de aer.
Fenotip - suma caracteristicilor demografice, clinice și fiziopatologice. Documentul enumeră cele mai frecvente fenotipuri, care ajută clinicienii. Acest lucru este, de asemenea, util pentru medicii generaliști în recunoașterea bolii în rândul pacienților lor, chiar și în absența unui panou de diagnostic complet.
- Astmul alergic - cel mai ușor de recunoscut, este adesea în copilărie. Examinarea sputei înainte de tratament indică inflamație eozinofilă. Datele privind ereditatea sau eczema, rinita alergică, alergia la alimente sau medicamente susțin acest fenotip. Răspuns bun la terapia ICS (corticosteroizi inhalatori).
- Astm non-alergic - Unii adulți au astm fără alergie. Examinarea sputei arată prezența neutrofilelor, eozinofilelor. Pacienții cu astm non-alergic au adesea un răspuns mai slab la tratamentul ICS.
- Astm cu restricție fixă a fluxului de aer - Unii pacienți cu astm de lungă durată dezvoltă restricție fixă a fluxului de aer, care se crede că se datorează remodelării peretelui căilor respiratorii.
- Astm și obezitate - unii pacienți cu obezitate și astm au afecțiuni respiratorii severe și inflamații minore eozinofile ale căilor respiratorii.
Masa. 1. Criterii de diagnostic
Caracteristici de diagnostic
Criterii pentru diagnostic
senzație de apăsare a pieptului și tuse
Simptomele variază în timp și intensitate;
Agravarea simptomelor pe timp de noapte și în timpul lucrului;
Simptomele sunt adesea provocate de efort, râs, alergeni, aer rece;
Și
La copii peste 13%
200 ml între vizite și fără dovezi de infecție
Capitolul doi: Evaluarea astmului
- Evaluarea astmului se realizează în două direcții: controlul simptomelor și al factorilor de risc.
- Funcția pulmonară nu mai este utilizată ca parametru pentru controlul astmului, ci ca mijloc de stratificare a riscului inițial și pe termen lung.
- Severitatea astmului este stabilit retrospectiv în funcție de necesitățile tratamentului, ducând la controlul simptomelor.
- Instrumente practice:
- Scala de evaluare a controlului astmului, inclusiv factorii de risc;
- Algoritm clinic pentru a distinge între astmul refractar necontrolat și sever.
Abordarea combinată a evaluării astmului prin „controlul simptomelor” (care combină - simptome, treziri nocturne, utilizarea medicamentelor - agoniști β2 inhalatori, metilxantine și anticolinergice, limitarea activității) și „complicații viitoare” (risc de exacerbări, dezvoltare de restricționarea fluxului de aer sau apariția efectelor secundare adverse datorate medicamentelor utilizate) se datorează faptului că diferite fenotipuri și regimuri de tratament prezintă o nepotrivire între simptome și riscul de complicații. În fenotipul alergic tipic, nu se observă o astfel de disonanță între abordarea convențională a tratamentului cu corticosteroizi inhalatori (ICS) și apariția complicațiilor. Îmbunătățirea pe termen scurt a simptomelor este însoțită de obicei de reducerea pe termen lung a exacerbărilor. Într-o altă situație, utilizarea placebo sau a monoterapiei cu agoniști β2 cu acțiune îndelungată (LABA) poate reduce simptomele fără a reduce riscul de exacerbare.
Evaluarea astmului se realizează în două direcții: controlul simptomelor și al factorilor de risc. Acest lucru a necesitat înlocuirea termenului „control clinic” cu „control al simptomelor”. Șablonul de evaluare a astmului conține o listă extinsă de factori de risc variați și fixi care sunt predictori ai evenimentelor adverse viitoare. Această proprietate este independentă de simptomele disponibile.
Odată ce astmul a fost diagnosticat, spirometria este utilizată în primul rând pentru a identifica pacienții cu risc crescut de exacerbări. Valorile FEV1 la persoanele sănătoase indică fluctuații de 12% atunci când sunt măsurate în două săptămâni consecutive și cu 15% între doi ani consecutivi. Aceste valori sunt crescute la pacienții cu patologie pulmonară. Acest lucru limitează semnificativ utilizarea FEV1 ca indicator al unei modificări a abordării tratamentului. Următoarele situații susțin, de asemenea, acest lucru: există plângeri semnificative ale funcției pulmonare normale. În această situație, este adecvat să se ia în considerare un diagnostic alternativ, cum ar fi disfuncția cordului vocal. În situația opusă, prezența a câteva afecțiuni cu funcție pulmonară redusă ar trebui să evalueze probabilitatea de dificultate de adaptare la funcția pulmonară redusă sau la stilul de viață sedentar.
Debitul expirator de vârf (VED) este utilizat pentru o perioadă scurtă de timp în diagnosticul de astm. De exemplu, în astmul legat de muncă, pentru a specifica factorii cauzali, exacerbările și răspunsul la tratament. Monitorizarea pe termen lung a DEV este utilizată în principal la pacienții cu astm bronșic sever, la cei cu dificultăți de adaptare la funcția pulmonară redusă.
Severitatea astmului este determinată după câteva luni de tratament. Algoritmul clinic pentru a distinge între astmul refractar necontrolat și sever este orientat pragmatic cu o evaluare inițială a tehnicii adecvate de inhalare (aproximativ 80% dintre pacienți nu au) sau nerespectarea recomandărilor (aproximativ 50% dintre pacienți).
Masa. 2. Evaluarea controlului astmului
Controlul simptomelor, care acoperă o perioadă din ultimele 4 săptămâni
controlat: 0 puncte
controlat parțial: 1-2 puncte
Capitolul trei: Tratament pentru controlul simptomelor și minimizarea riscului de complicații viitoare
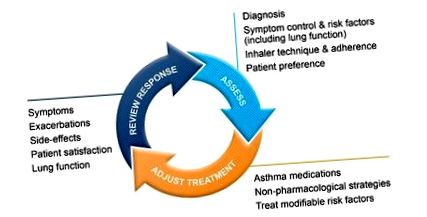
- A fost dezvoltat un ciclu de tratament de control. Acesta include următorii pași: evaluați și ajustați tratamentul, reevaluați răspunsul.
- Abordarea individuală a fiecărui pacient.
- Noi indicații pentru tratamentul de control inițial, inclusiv astmul ușor.
- Înainte de a lua în considerare luarea unui pas în abordarea terapeutică, diagnosticul pacientului, tehnica de inhalare și cooperarea ar trebui reevaluate.
Tratamentul astmului este un ciclu continuu: o evaluare inițială a unei strategii terapeutice, urmată de o ajustare a abordării, care include tratament farmacologic și non-farmacologic, urmată de o reevaluare a răspunsului. Toate acestea se realizează prin construirea unui parteneriat între profesioniștii din domeniul medical și pacienți, care se reflectă în formarea continuă în abordarea corectă a inhalării, aportul adecvat al medicamentului în doză terapeutică completă, instruirea pentru autotratarea țintită prin dezvoltarea unui plan de acțiune individual. . Se pune accent pe îmbogățirea cunoștințelor de sănătate ale pacienților. Se recomandă vorbirea lentă, limitarea limbajului medical și conceptele numerice. Destinat prioritizării informațiilor atunci când prezintă pacientul de la cel mai important la cel mai puțin important.
Au fost extinse indicațiile pentru tratamentul cu doze mici de ICS în etapa 1. Motivul utilizării acestora sunt datele din studiul START. Au fost raportate jumătate din decesele cauzate de astm și spitalizări. În studiu, jumătate dintre pacienți au prezentat reclamații mai puțin de două ori pe săptămână. Pe de altă parte, nu există dovezi concrete care să susțină monoterapia cu SABA. Recomandările GINA pentru terapia cu SABA în monoterapie sunt la pacienții cu simptome mai mici de două ori pe lună, fără treziri nocturne în luna precedentă, fără factori de risc pentru exacerbare și fără exacerbări severe în anul precedent. La acest nivel de simptome (pasul 1) este indicată utilizarea ICS. Motivul este reducerea riscului de exacerbări severe.
Pașii 3 și 4 enumeră două moduri combinate „preferate” ICS/LABA. Acestea sunt doze mici de budesonidă/formoterol și beclometazonă/formoterol. Actualizarea GINA 2015 indică locul utilizării ceații de aerosoli tiotropium în etapele 4 și 5 ca tratament de întreținere adjuvantă la pacienții cu vârsta ≥ 18 ani tratați cu o combinație de întreținere a corticosteroizilor inhalatori ≥ 800 µg budesonidă zilnic sau echivalent. β2 agoniști și în prezența uneia sau mai multor exacerbări în ultimul an.
Luarea în considerare a scăderii comportamentului terapeutic este după trei luni de menținere a unui control bun. Este important să alegeți momentul potrivit pentru aceasta - fără prezența infecției, sarcinii, fără o schimbare a mediului social.
FIG. 1. Ciclul de tratament pentru astm bazat pe control
Nu toți factorii de risc, în special variabilele, sunt o indicație pentru a face un pas în strategia de tratament. Acesta este cazul, de exemplu, cu obezitatea sau fumatul. Recomandările sunt pentru pierderea în greutate și renunțarea la fumat și apoi reevaluarea comportamentului terapeutic.
abl. 3. Factori de risc
FEV1 trebuie măsurat la începutul tratamentului.
Măsurarea ulterioară după 3 până la 6 luni, tratând și documentând cel mai bun rezultat pentru pacientul respectiv.
• Simptome astmatice necontrolate
• Utilizarea crescută a SABA (mortalitate crescută atunci când este utilizat peste 1 pachet de 200 de doze pe lună)
• Utilizarea necorespunzătoare a ICS - nu este prescrisă; tehnica de inhalare necorespunzătoare și/sau aportul necorespunzător
• FEV1 scăzut, în special 1 Prezența unuia sau mai multor factori de risc crește riscul de exacerbări, chiar și cu un control bun al simptomelor
Capitolul patru: Tratamentul astmului bronșic exacerbat și exacerbat
- Tratamentul astmului bronșic agravat în ansamblu (plan de acțiune scris, tratament în asistența medicală primară, secția de urgență, urmărire după fiecare exacerbare).
- „Exacerbare” este termenul preferat atunci când vorbești cu pacientul.
- Identificați pacienții cu risc crescut de deces cauzat de astm. Se recomandă examinări mai frecvente.
- Creșterea rapidă și rapidă a ICS.
- Simplificarea severității astmului acut după cum urmează: ușoară/moderată, severă și care pune viața în pericol.
- Recomandări revizuite pentru oxigenoterapie - datorită datelor despre hipercapnie și evenimentelor adverse în aprovizionarea cu oxigen cu flux mare; valorile țintă pentru saturația de oxigen sunt de 93% - 95% (la copii cu vârsta cuprinsă între 6 - 11 ani 94-98%).
- După orice exacerbare severă, trebuie instituit sau reluat tratamentul de întreținere cu ICS. Fiecare exacerbare severă crește șansa de reapariție în următoarele 12 luni, iar riscul rehospitalizării este redus cu 40% cu utilizarea regulată a ICS.
Se recomandă creșterea precoce a dozei de ICS pe baza unei revizuiri a tuturor dovezilor aplicabile. Dublarea dozei de ICS pentru agravarea astmului este recomandată în ghidurile anterioare de tratament pentru astm. Datele din trei studii randomizate nu au demonstrat eficacitate în dublarea dozei de ICS la pacienții tratați cu terapia de întreținere a ICS, cu excepția cazurilor cu doze mari de ICS. Acest lucru a dus la o schimbare rapidă în multe ghiduri de tratament. Sa considerat suficientă creșterea dozei de SABA până când s-a realizat o astfel de agravare a exacerbării, încât au fost necesari corticosteroizi sistemici. O creștere timpurie a ICS poate fi prescrierea ICS, o creștere pe termen scurt a dozei unui ICS deja prescris sau adăugarea unui nou ICS. Rațiunea acestui comportament este că majoritatea exacerbărilor se caracterizează prin inflamație crescută. Conform lui Oborne J, Mortimer K, Hubbard RB și colab. o creștere de patru ori a ICS într-un timp scurt reduce riscul de exacerbări severe.
Capitolul cinci: Diagnosticul și tratamentul inițial al astmului - sindromul BPD care se suprapune
- Un nou capitol care oferă sfaturi practice pentru medicii non-respiratori. Este, de asemenea, subliniată necesitatea mai multor studii pentru tratarea pacienților cu astm și BPOC.
- O abordare distinctă în îngrijirea primară pentru astm, BPOC și sindromul suprapus.
- Recomandări pentru un tratament inițial sigur.
Formele tipice de astm și BPOC se disting clar. Sindromul respirator cronic, în special la adulții cu antecedente de fumat pe termen lung, poate fi problematic dacă combină caracteristicile ambelor boli. Motivul pentru aceasta este faptul că cele două boli nu se exclud reciproc. La fel ca și opinia generală că sunt boli eterogene. Incidența ACOS (sindromul de suprapunere a astmului-BPOC) este cuprinsă între 15% și 55%. Cifrele variază în funcție de definiția utilizată în studiile populației. Liniile directoare comportamentale pentru astm și BPOC conțin strategii opuse pentru un tratament sigur.
În astm, utilizarea tratamentului cu ICS este baza. Motivul este efectul lor semnificativ în reducerea mortalității, internărilor și simptomelor. Există dovezi puternice împotriva utilizării LABA ca monoterapie (fără ICS) din cauza riscului de exacerbări severe și de deces cauzat de astm.
În schimb, în BPOC moderată, se recomandă monoterapia cu LABA, iar terapia ICS singură este evitată datorită datelor scăzute privind beneficiile/riscurile.
Majoritatea studiilor nu includ pacienții cu ACOS, ceea ce împiedică obținerea unor dovezi suficiente. Pacienții cu sindrom suprapus au perspective clinice mai slabe comparativ cu pacienții diagnosticați cu astm sau BPOC.
Masa. 4. Caracteristicile astmului, BPOC și ACOS
Caracteristică
Astm
BPOC
ACOS
[1] * Strategia globală pentru gestionarea și prevenirea astmului (ACTUALIZARE 2015)
Conectați-vă sau înregistrați-vă gratuit pentru a accesa conținutul complet și articolele revistei în format PDF.
- Primarul municipiului Vidin, Dr. Tsvetan Tsenkov, va participa la sărbătoare cu ocazia deschiderii noului
- Cum să țineți colesterolul și tensiunea arterială sub control
- Lubo Kirov și-a prezentat noua piesă; Poti; (VIDEO)
- Dragostea îl emoționează pe noul partener de ecran al lui Viktor Nikolaev îl înjunghie pe cameraman (Foto)
- Bulgaria protestează și împotriva noii enciclopedii macedonene - Bulgaria