Termenul „gastrită” a fost folosit pentru prima dată în 1728 de medicul german Georg Ernst Stahl pentru a descrie inflamația mucoasei stomacului - cunoscută acum ca fiind secundară afectării mucoasei (adică deteriorarea și regenerarea celulelor). În trecut, mulți credeau că gastrita este o constatare histologică utilă, dar nu o boală. Toate acestea s-au schimbat odată cu descoperirea Helicobacter pylori de către Robin Warren și Barry Marshall în 1982, ceea ce a dus la identificarea, descrierea și clasificarea multor gastrite diferite.
Gastrita cronică este o boală în primul rând a adulților. Poate fi găsit și la copii. Cauzat de factori exogeni:
- erori alimentare
- alcoolismul cronic
- fumat
- consumând alimente calde și picante
- utilizarea pe termen lung a medicamentelor (acetizal, salicilați, corticosteroizi etc.)
Factorii endogeni includ hipoxia cronică în decompensarea cardiacă, procesele autoimune, tulburările neuroendocrine, stresul, gastrita acută recurentă.
Apariția și dezvoltarea gastrită cronică se explică prin participarea diferitelor mecanisme: imunitar, alcoolic, antiinflamatoare nesteroidiene, reflux duodeno-gastric, infecție cu Helicobacter-pylori.
Pe baza principiilor clinice și morfologice în diagnosticul biopsiei și a recomandărilor sistemului Sydney pentru clasificarea gastritei, gastrita cronică este prezentată în următoarele forme principale: gastrită cronică fără atrofie și gastrită atrofică cronică.
În funcție de locație, gastrita cronică poate fi localizată în zona antrului și în corpul stomacului.
În funcție de cauza etiologică, gastrita cronică poate fi asociată cu Helicobacter-pylori, bacteriană, virală, fungică, reactivă (reflux, alcool, medicamente).
Formele speciale de gastrită cronică sunt:
- granulomatos - tuberculoză
- asociată cu sarcoidoză
- asociat cu boala Crohn
- eozinofil
- alergic
- idiopatic (de etiologie necunoscută)
Gastrita chimică sau reactivă este cauzată de deteriorarea mucoasei stomacului ca urmare a refluxului de bilă și secreții pancreatice în stomac, dar poate fi cauzată de substanțe exogene, inclusiv antiinflamatoare nesteroidiene, acid acetilsalicilic, agenți chimioterapeutici și alcool . Aceste substanțe chimice provoacă leziuni epiteliale, eroziuni și ulcere, urmate de hiperplazie regenerativă, care poate fi detectată ca hiperplazie foveolară și leziuni capilare, cu edem al mucoasei, hemoragie și creșterea mușchilor netezi în lamina propria cu inflamație minimă sau deloc.
Gastrita H. pylori este o infecție gastrică majoră și este cea mai frecventă cauză a gastritei cronice, infectând 50% din populația lumii. Cazurile de gastrită cronică documentată histologic sunt diagnosticate ca gastrită cronică de etiologie necunoscută sau gastrită de tip nedeterminat, atunci când niciunul dintre rezultate nu reflectă vreunul dintre modelele de gastrită descrise și o cauză specifică nu poate fi identificată.
Helicobacter pylori este principala cauză de gastrită cronică, ulcer peptic, adenocarcinom gastric și limfom gastric primar. Bacteriile supraviețuiesc în stratul mucos care acoperă epiteliul suprafeței stomacului și părțile superioare ale foveei gastrice. Infecția este de obicei dobândită în timpul copilăriei. Odată prezentă în stomac, bacteria trece prin stratul mucoasei și se așează pe suprafața luminală a stomacului, provocând un răspuns inflamator puternic în țesutul subiacent.
Prezența H. pylori este asociată cu afectarea țesuturilor și detectarea histologică a gastritei active și cronice. Răspunsul gazdei la H. pylori și produsele sale bacteriene constă din limfocite T și B, denotând gastrită cronică, urmată de infiltrarea laminei proprii și a epiteliului gastric de către leucocite polimorfonucleare, care în cele din urmă fagocitează bacteriile.
Interacțiunea H. pylori cu mucoasa superficială duce la eliberarea interleukinei-8, ceea ce duce la acumularea de leucocite polimorfonucleare și poate începe întregul proces inflamator. Celulele epiteliale gastrice exprimă molecule de clasa II care pot spori răspunsul inflamator prin prezentarea de antigeni H. pylori, ducând la activarea mai multor factori de transcripție. La rândul său, aceasta duce la eliberarea ulterioară de citokine.
Nivelurile de leucotriene sunt, de asemenea, destul de ridicate, în special nivelul leucotrienei B4, care este sintetizat de neutrofilele gazdei și este citotoxic pentru epiteliul gastric. Acest răspuns inflamator duce la modificări funcționale în stomac, în funcție de zonele afectate ale stomacului. Când inflamația afectează mucoasa stomacului, celulele parietale sunt inhibate, ducând la secreția acidă redusă. Inflamația prelungită duce la pierderea celulelor parietale și o scădere a secreției acide devine permanentă.
Inflamația antrală modifică interacțiunea dintre gastrină și secreția de somatostatină, afectând celulele G (celule secretoare de gastrină) și celulele D (celule secretoare de somatostatină), respectiv. În special, secreția de gastrină este anormală la persoanele infectate cu H. pylori, cu stimulare dietetică excesivă care eliberează gastrină, care este cea mai importantă anomalie.
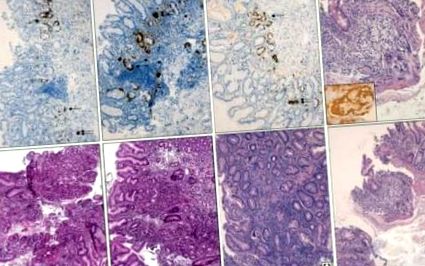
Gastrita asociată cu H. pylori poate prezenta niveluri diferite de severitate. Organismele H pylori se găsesc în stratul de mucoasă gastrică și se acumulează adesea în grupuri pe partea apicală a celulelor de suprafață gastrică, uneori în părțile inferioare ale foveolului gastric și rar în zonele mai profunde ale mucoasei asociate cu celulele glandulare (Figura 1 ).
Pacienții cu infecții tipice dezvoltă inițial gastrită cronică activă, în care H. pylori este observat atât în antrum, cât și în corpus. Leucocitele polimorfonucleare se infiltrează în lamina propria, glandele, epiteliul superficial și epiteliul foveolar, turnându-se uneori în lumen și formând microabcese mici. Au fost observate agregate limfoide și, uneori, foliculi limfoizi bine dezvoltați, care extind lamina proprie a mucoasei și limfocitele individuale pătrund în epiteliu.
Într-o boală cu o durată mai lungă, există o pierdere semnificativă a glandelor gastrice, o afecțiune cunoscută sub numele de atrofie gastrică. Atrofia gastrică poate rezulta din pierderea celulelor epiteliale gastrice care nu au fost înlocuite cu proliferarea celulară adecvată sau poate fi rezultatul înlocuirii epiteliului cu epiteliu de tip intestinal (metaplazie intestinală).
În stadiile avansate de atrofie asociate cu infecția cronică cu H. pylori, atât corpusul, cât și antrul prezintă o înlocuire extinsă cu metaplazie intestinală, care este asociată cu dezvoltarea hipoclorhidriei. Odată cu extinderea metaplaziei intestinale, numărul organismelor H. pylori găsite în stomac scade, deoarece bacteria este exclusă din zonele epiteliului metaplastic.
Modificările histologice ale gastritei atrofice autoimune variază în diferite stadii ale bolii. În faza incipientă, s-au observat infiltrarea multifocală difuză a laminei proprii de către celulele mononucleare și eozinofile și infiltrarea focală cu celule T a glandelor producătoare de acid. Au fost raportate, de asemenea, hiperplazia focală a mucoasei (metaplazia pseudopilorică) și modificările hipertrofice ale celulelor parietale.
În timpul fazei roșii a bolii, se observă o inflamație limfocitară crescută, atrofia glandei producătoare de acid și metaplazie intestinală focală. Etapa finală se caracterizează prin implicarea difuză a corpusului și fundului gastric prin gastrita atrofică cronică asociată cu metaplazia intestinului subțire. Antrul este cruțat.
Gastrita granulomatoasă afectează în principal antrul gastric. În primele etape, singurele constatări pot fi granuloamele izolate în mucoasă și submucoasă. În etapele ulterioare ale bolii, inflamația se extinde la muscularis propria, iar fibroza poate fi vizibilă. Granuloamele asociate tuberculozei sunt de obicei cazeoase. Granuloamele slab formate pot fi observate și în afectarea sifilitică a stomacului în stadiul terțiar al bolii.
Cauzele neinfecțioase ale granuloamelor gastrice duc, de obicei, la granuloame neîncazante. Astfel de cauze includ boala Crohn, sarcoidoza și granuloamele izolate.
Boala Crohn, care afectează stomacul, constă în inflamații inegale cu abcese. Agregatele limfoide sunt frecvente. Cazurile severe pot prezenta fisuri, ulcere, inflamații transmurale și fibroză seroasă și submucoasă. Se pot observa granuloame epitelioide bacteriene. Se produce infiltrare inflamatorie difuză a laminei proprii și atrofie glandulară. Implicarea stomacului este aproape întotdeauna sincronă cu boala Crohn în ileon sau colon.
Sarcoidoza și granuloamele izolate se caracterizează prin granuloame slabe cu inflamație ușor asociată. Deși sarcoidoza care afectează stomacul coexistă cu sarcoidoza care implică alte organe, gastrita izolată granulomatoasă afectează numai stomacul și este un diagnostic de excludere.
Infecția cu citomegalovirus a stomacului este observată la pacienții cu imunosupresie. Din punct de vedere histologic, s-au găsit incluziuni tipice eosinofile intranucleare și uneori incluziuni intracitoplasmatice mai mici (Figura 2). Infiltratul inflamator neuniform, ușor, se observă în lamina propria. Incluziunile virale sunt prezente în celulele epiteliale gastrice și în celulele endoteliale sau mezenchimale din lamina propria. Necroza mucoasei severe poate duce la ulcerații severe.
În gastrita eozinofilă, mucoasa prezintă o infiltrație intensă de numeroase eozinofile, cu abcese ocazionale. Infiltratul conține de obicei 10-50 de eozinofile pe câmp de mare putere, precum și celule plasmatice. Pot exista umflături ale mucoasei, congestie și necroză a epiteliului superficial cu eroziuni mici. Infiltrarea mucoasă de către un infiltrat eozinofilic în bandă în partea inferioară a laminei proprii deasupra mucoasei musculare caracterizează gastroenterita eozinofilă asociată cu tulburări ale țesutului conjunctiv.
În gastrita limfocitară, lamina propria este infiltrată de un număr mare de limfocite T mature mature. Limfocitele T abundente pătrund de obicei în epiteliul superficial. Diagnosticul se poate face atunci când sunt observate 30 sau mai multe limfocite la 100 de celule epiteliale consecutive și se recomandă numărarea biopsiei gastrice.
În gastrita cu radiații, radiația provoacă modificări degenerative în celulele epiteliale și infiltrat inflamator cronic nespecific în lamina propria. Aceste modificări sunt reversibile pe o perioadă de câteva luni. Cantități mai mari de radiații provoacă leziuni permanente mucoasei, cu atrofia glandelor fundului, eroziuni ale mucoasei și hemoragie capilară.
Gastrita granulomatoasă idiopatică prezintă o histopatologie similară cu gastrită cronică în sarcoidoză. Îngustarea antrală are loc din cauza inflamației transmurale, tubeless, granulomatoase. Inflamația și fibroza sunt de obicei limitate la mucoasă. Gastrita granulomatoasă idiopatică poate fi formă izolată sau limitată de sarcoid gastric sau boala Crohn.
Gastrita cronică fără atrofie are o caracteristică specifică. Microscopic, grosimea mucoasei gastrice este în limite normale. La unii pacienți, datorită umflăturii și infiltrării inflamatorii, mucoasa poate fi ușor mărită. Epiteliul tapițeriei este cilindric, dar pe alocuri devine inferior, cubic. Limita dintre celule este clară. Există modificări degenerative în citoplasmă (în special degenerescența proteinelor). Nucleii sunt dislocați, unii sunt împinși afară, cu aspect picnotic, iar în puțuri sunt mai mari și mai luminoase. Gropile în sine sunt localizate uniform (ritmic), unele doar mai puțin adânci sau, dimpotrivă, mai profunde, curbate. Nu s-au observat modificări în corpus și glandele antrale.
Uneori pot fi observate patru fenomene morfologice de valoare diagnostică importantă la nivelul gâtului și corpului glandelor corpusului:
- Mucoidizarea glandelor - în unele cazuri crește cantitatea de celule mucinoase din colul uterin și corpul glandelor corpusului, în care acestea înlocuiesc o parte din celulele principale și parietale.
- Transformarea pseudopilorică - cu înlocuirea completă a celulelor specializate cu cele mucinoase. Există o reorganizare structurală a mucoasei corpusului de tip pseudopiloric.
- Metaplazie intestinală (reconstrucție structurală de tip intestinal) - în epiteliul superficial și/sau în profunzimea corpului și în antrum, se pot găsi focare excepțional de mici de reconstrucție structurală de tip intestinal.
- Parietalizarea glandelor corpusului - crește de până la 1,5 ori numărul de celule parietale.
Gastrita atrofică cronică are, de asemenea, particularitățile sale. La el, mucoasa gastrică apare palidă, strălucitoare, adesea cu transluciditatea vaselor submucoase. Relieful său este mai mult sau mai puțin neted și are un aspect marcat subțire. Microscopic, fântânile sunt lărgite și deformate, cu o formă specială de pinten sau sunt foarte puțin adânci, aproape netezite, ceea ce le face să arate în general reduse. În alte cazuri, ele devin adânci și pliurile ies în afară, ca firele de păr intestinale subțiri (calomnie).
Epiteliul tapițat este scăzut, cubic, cu nuclei hipercromici, uneori cu multiplicitate pronunțată, mai ales în gropi. Celule mai mari, luminoase, dispuse în mai multe rânduri cu nuclee și nuclee ușoare, pot fi, de asemenea, văzute aici (Figura 3). Glandele își pierd ordinea normală, scad în număr și diverg datorită creșterii țesutului conjunctiv între ele. Printre glande se pot observa fibre musculare netede reticulare și mai moi. Stratul muscular al mucoasei este îngroșat de mai multe ori.
Infiltratul inflamator acoperă difuz întreaga grosime a mucoasei până la stratul său muscular, intrând în ea. Limfocitele și celulele plasmatice domină. Cadavrele lui Russell sunt adesea găsite. Limfocitele migrate, așa-numitele limfocite intraepiteliale, apar în epiteliul superficial și în groapă.
- Gastrita cronică la câini Competentă pentru sănătatea iLive
- Gastrită cronică, ICD K29 nespecificată
- Gastrita cronică și gastroduodenita la copii Competente pentru sănătatea iLive
- Cauzele gastritei cronice, simptomele, diagnosticul, tratamentul Competente pentru sănătatea iLive
- Gastrită cronică superficială ICD K29