Prof. Dr. G. Momekov, dr. Profesor asistent M. Kondeva-Burdina
Piracetam este prototipul așa-numitelor Medicamentele „nootropice” cu principala caracteristică a afectării funcțiilor cognitive (ca urmare a îmbătrânirii creierului, a hipoxiei, a reducerii glucozei din creier, a afectării creierului și chiar a neurodegenerării) fără sedare și excitare. Toate aceste procese patologice sunt asociate cu așa-numitele. „Cercul vicios” între stresul oxidativ indus - producția crescută de radicali liberi - deteriorarea mitocondrială - producția redusă de energie pentru celulă - producția crescută de radicali liberi.
În pofida istoriei de 50 de ani și a utilizării clinice de zece ani a Piracetam, detaliile farmacologiei sale rămân neclare, studiile efectuate în ultimii ani necesitând o reevaluare finală a proprietăților farmacodinamice. În prezent, conceptul de farmacologie al piracetamului s-a schimbat radical de la un medicament cu un mecanism de acțiune non-selectiv membrana-tropic, deoarece este considerat un agent multimodal și mai multe ținte farmacologice bine validate. Această prezentare își propune să ofere o scurtă prezentare generală a proprietăților farmacodinamice ale Piracetam prin prisma noilor date privind mecanismul său de acțiune și traducerea clinică potențială a acestor proprietăți.
Istorie
Piracetam a fost sintetizat pentru prima dată în 1964 de UCB, Belgia. În 1965, au fost efectuate studii clinice asupra efectelor bolii de călătorie, vertijului, nistagmusului și epilepsiei copilăriei. În perioada 1968-1971 au fost studiate efectele sale asupra capacităților de memorie în hipoxie și amnezie indusă de electroșoc, iar în 1971 în Franța a fost introdus în practica clinică. În 1973, Corneliu E. Giurgea a creat conceptul de medicamente nootrope. Se bazează pe farmacologia piracetamului și se referă la medicamente care cresc schimbul și transferul de informații intercerebrale fără a prezenta alte efecte farmacologice semnificative. Funcțiile cognitive (învățare și memorie - pe termen scurt și lung) depind în mare măsură de transferul de informații intracerebrale, în special în tulburări [1] .
Indicații clinice
Piracetam este indicat în prezent pentru:
- tratamentul simptomatic al sindromului psihoorganic cu următoarele manifestări: tulburări de memorie și atenție, lipsă de motivație;
- tratamentul mioclonului cortical, singur sau în combinație;
- tratamentul vertijului și a dezechilibrelor asociate, cu excepția amețelilor de origine vasomotorie sau mentală.
La copii, este utilizat pentru tratarea dislexiei în combinație cu măsuri adecvate, cum ar fi logopedia și pentru prevenirea și remisiunea crizei vasoocluzive cu celule secerătoare.
Proprietăți fizico-chimice, farmacocinetică și toxicitate acută preclinică
Piracetamul este foarte hidrofil, nu este metabolizat și este eliminat nemodificat prin urină. Deoarece nu interacționează cu sistemul citocromului P450, nu se cunosc interacțiuni medicamentoase relevante clinic la nivel de biotransformare. Caracteristicile sale farmacocinetice sunt sintetizate în tabel. 1. Piracetamul este practic netoxic, cu un LD50 de peste 10 g/kg greutate corporală la șobolani [2] .
Volumul distribuției - VD
Farmacodinamica
Piracetamul este un medicament nootrop care este un derivat al acidului gamma-aminobutiric (GABA). Deși sintetizat ca un analog ciclic al acestui neurotransmițător, Piracetam nu se leagă de receptorii GABA și nu afectează absorbția sinaptozomală a GABA [1]. .
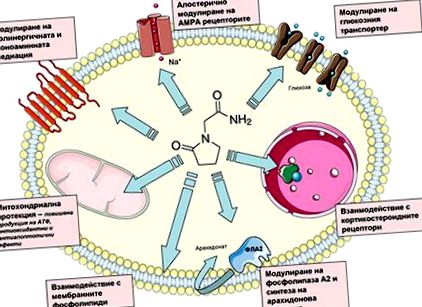
Până de curând, Piracetam a fost considerat doar ca un modulator nespecific al structurii și funcției membranei, deoarece se leagă nespecific de capătul polar al fosfolipidelor de membrană și astfel crește fluiditatea membranei. Acest efect este mai pronunțat în disfuncțiile deja manifestate, cum ar fi legate de vârstă. Se știe că neurotransmisia este modulată de fluiditatea membranei, un mecanism care explică farmacologia independentă de transmițător a Piracetamului. În ultimii ani, cu toate acestea, au existat dovezi solide că Piracetam interacționează cu o varietate de structuri celulare, inclusiv unii receptori, transportori de membrană și enzime, ceea ce necesită o regândire a conceptului proprietăților sale farmacodinamice (Fig. 1).
Țintă farmacologică - receptori glutamatergici AMPA
Astăzi, receptorii glutamatergici AMPA sunt cea mai importantă țintă farmacologică calificată a Piracetamului. S-a constatat că afectează selectiv receptorii AMPA implicați în procesul neurofiziologic de formare și consolidare a memoriei [2]. .
Modularea medierii glutamatergice - NMDA
Piracetam restabilește reducerea legată de vârstă a numărului de receptori NMDA (M-metil-D-aspartat) și colinergici de pe membrana neuronală. Receptorii NMDA sunt un tip de receptor ionotrop, deosebit de important pentru procesele de învățare și memorie. Se leagă de neurotransmițătorii excitatori, cum ar fi glutamatul, iar activarea lor este unul dintre primii pași în procesele de memorie. Restabilește neurotransmisia suprimată (susține activitatea unui număr de sisteme de neurotransmițători precum colinergice, noradrenergice și dopaminergice) [3] .
FIG. 1. Reprezentarea schematică a principalelor proprietăți farmacodinamice ale Piracetamului, care determină activitatea sa neuroprotectoare și influența funcțiilor cognitive. Proprietățile vasculare și hematoreologice nu sunt prezentate (vezi textul pentru detalii).
Modularea medierii colinergice
Piracetamul reduce sau blochează complet efectul amnestic și consumul redus de glucoză indus de scopolamină. La doze mici (3-100 mg/kg i.p., la șobolani) a crescut transportorul de colină cu afinitate ridicată (HACU) în sinaptozomii hipocampici, în timp ce la doze mari efectele au fost contradictorii. Reduce amnezia, dar potențează epuizarea acetilcolinei indusă de hemicolin-3. Stimulează eliberarea acetilcolinei în hipocampul șobolanului și antagonizează efectele letale ale hemicolinului-3 și blocul neuromuscular al d-tubocurarinei la pisici, care este cel mai probabil asociat cu stimularea sintezei acetilcolinei datorită efectelor asupra HACU.
Tratamentul cronic cu Piracetam (500 mg/kg 1-2 săptămâni p.o., șobolani) crește densitatea și sensibilitatea receptorilor muscarinici la șobolani tineri și adulți [3]. .
Modularea medierii monoaminei
Deși Piracetam nu este un agonist al receptorilor de monoamină, s-a constatat că intervine în mod cuprinzător în procesele de eliberare de dopamină, norepinefrină și serotonină, interacțiunea lor cu structurile receptorilor și catabolismul lor. S-a constatat că piracetamul duce la creșterea excitabilității neuronilor noradrenergici în locus coeruleus la șobolani și la creșterea metabolismului norepinefrinei în trunchiul cerebral. Doze mari de Piracetam (600 mg/kg p.o., 5 zile, șobolani) au antagonizat efectul amnestic al inhibitorului hidroxilazei etilxantogenat de sodiu. Crește eliberarea și metabolismul dopaminei, dar nu modulează absorbția serotoninei.
Doze foarte mari de Piracetam (5 g/kg i.p. timp de 14 zile) au modificat nivelurile de norepinefrină, dopamină și serotonină în diferite regiuni ale creierului la șobolani. De exemplu, sa constatat că Piracetam reduce scăderile legate de vârstă ale nivelurilor de monoamină la șobolanii mai în vârstă. La o doză de 600 mg/kg pe zi timp de 30 de zile, Piracetam a redus activitatea MAO in vivo cu 20%, în timp ce in vitro la o concentrație de 100 mM a inhibat MAO. Un alt studiu a arătat inhibarea MAO A și MAO B în striat, dar stimularea în hipocampus, efectul total fiind stimularea [3]. .
Modularea memoriei
După cum sa menționat mai sus, Piracetam modulează pozitiv receptorii AMPA implicați în procesul neurofiziologic de formare și consolidare a memoriei. Crește activitatea fosfolipazei A2 necesară pentru producția neuronală de acid arahidonic și, după cum știm, prostaglandinele modulează excitabilitatea neuronală și transmisia neuronală sinaptică.
Efectele cognitive ale Piracetamului sunt îmbunătățite în combinație cu colina, probabil datorită nevoilor crescute induse de Piracetam de sinteză a acetilcolinei [4,5] .
Modularea funcțiilor cognitive
Piracetam îmbunătățește funcția cognitivă la voluntarii sănătoși sub hipoxie (n = 12) [6] .
Efecte asupra fosfolipidelor de membrană
Piracetam se leagă de grupurile polare ale bistratului fosfolipidic, provocând o reorganizare a moleculelor lipidice. Conduce la formarea unui complex medicament-fosfolipid și restabilește integritatea membranei. Pe de altă parte, îmbunătățește funcțiile sinaptice și mitocondriale, crește potențialul membranei mitocondriale, nivelurile de ATP și reduce sarcina β-amiloidă [7,8,9] .
Modularea proprietăților reologice ale sângelui
Piracetamul inhibă în general agregarea plachetară, dar la pacienții cu boli care duc la creșterea agregării plachetare, acesta îl normalizează. Eficacitatea sa este similară cu acidul acetilsalicilic în prevenirea secundară a accidentului vascular cerebral ischemic. Eficacitatea clinică a fost stabilită și la pacienții cu fenomen Raynaud [10]. .
Modularea stresului oxidativ
Piracetamul nu este un antioxidant sau eliminator de radicali liberi, dar sa demonstrat că modulează efectele toxice în condiții de stres oxidativ sau nitrosativ. Administrat la o doză de 500 mg/kg/zi timp de 2 săptămâni pentru a proteja disfuncția mitocondrială cauzată de peroxid de hidrogen sau nitroprusid de sodiu [15].
Modularea apoptozei (moarte celulară programată)
Activarea caspazei 9 duce la activarea caspazei 3 și la apariția apoptozei. În culturile de celule neuronale, caspaza 9 a fost activată după 2 ore de tratament cu nitroprusidă de sodiu. Pre-tratamentul cu piracetam a dus la o reducere semnificativă statistic a activității caspazei 9 [15]. .
Modularea transportului glucozei
O serie de medicamente, hormoni și boli afectează absorbția glucozei și metabolismul din creier. Medicamentele nootrope au o structură similară cu TRH (hormonul care eliberează tirotropina), care s-a dovedit că crește absorbția glucozei în creier, cel mai probabil mecanismul prin care medicamentele nootropice îmbunătățesc absorbția glucozei de către celule.
Piracetam îmbunătățește absorbția glucozei în celulele creierului la pacienții cu boala Alzheimer. Acest lucru are valoare terapeutică, deoarece acești pacienți au redus absorbția glucozei cu ani înainte de demență și au redus volumul cortical.
Piracetamul crește absorbția glucozei în celulele creierului șobolanilor tratați cu scopolamină.
Barbituricele, melatonina, fenotiazinele și diazepamul s-au arătat in vivo și in vitro pentru a reduce absorbția glucozei prin inhibarea transportului glucozei către creier. Transportul glucozei se îmbunătățește datorită fluidității crescute a membranei celulare [16,17,18] .
Modularea modificărilor morfologice în neuronii piramidali corticali
Pe măsură ce îmbătrânim, dendritele și terminalele sinaptice ale neuronilor individuali cresc pentru a compensa pierderea neuronală. Acest lucru nu se întâmplă în bolile neurodegenerative. Medicamentele nootropice stimulează neurotogeneza. Piracetam îmbunătățește neuritogeneza în linia celulară PC12 după tratamentul cu β-amiloid [19,20,21] .
- Cynical Speech ™; Totul este liniștit și liniștit pe frontul de est
- 5 beneficii ale consumului de sushi
- C-peptida Med
- Ceasul biologic • Russell Foster, Lyon Kreitzman • Editura; Est Vest
- Yamaha dezvăluie noul R1 pentru 2009