Coagularea intravasculară diseminată este un sindrom dobândit de activare a coagulării intravasculare care duce la deteriorarea vaselor de sânge mici și disfuncție severă a organelor. Coagularea intravasculară diseminată (sindromul Dick) se caracterizează prin activarea sistemică a coagulării sângelui, ceea ce duce la generarea și depunerea fibrinei, care duce la trombi microvasculari în diferite organe și contribuie la sindromul disfuncției organelor multiple.
Distrugerea sistemului fibrinolitic contribuie în continuare la formarea unui cheag intravascular, dar în unele cazuri fibrinoliza accelerată poate provoca sângerări severe. Prin urmare, un pacient cu coagulare intravasculară diseminată pot exista atât o problemă trombotică, cât și sângerări, ceea ce în mod evident complică tratamentul adecvat.
Coagularea intravasculară diseminată nu este în sine o boală specifică. Mai degrabă, este o complicație sau efect al progresiei altor boli. Este întotdeauna secundar și este asociat cu o serie de afecțiuni clinice, implicând de obicei activarea inflamației sistemice. Astfel de condiții includ următoarele:
- sepsis și infecție severă
- trauma
- boli maligne
- reacții grave de transfuzie
- complicații obstetricale - embolie cu lichid amniotic, abruptio placentae, eclampsie
- anomalii vasculare - sindromul Kasabach-Merritt și anevrisme vasculare mari
- insuficiență hepatică severă
- reacții toxice severe
- lovitură de căldură și hipertermie
- necroză hemoragică a pielii (purpura fulminans)
În funcție de rata de dezvoltare și de tipul de boală anterioară care duce la această afecțiune, coagularea intravasculară diseminată poate apărea ca sindrom DIC acut, subacut sau cronic.
Coagularea sângelui este un sistem autoreglat cu lanț care cuprinde trei faze. Rezultatul final este conversia fibrinogenului dizolvat în fibrină insolubilă. Fibrinoliza este procesul invers. În condiții fiziologice, coagularea și factorii anticoagulanți din sânge se află în echilibru dinamic, reglementat de mecanisme neuroendocrine. Când coagulare intravasculară diseminată procesele de coagulare a sângelui și fibrinoliza sunt perturbate.
În condiții homeostatice, corpul este menținut într-un echilibru fin de coagulare și fibrinoliză. Activarea cascadei de coagulare produce trombină, care transformă fibrinogenul în fibrină. Un cheag stabil de fibrină este produsul final al hemostazei. Sistemul fibrinolitic funcționează apoi pentru a distruge fibrinogenul și fibrina. Activarea sistemului fibrinolitic generează plasmină (în prezența trombinei), care este responsabilă pentru liza cheagurilor de fibrină. Degradarea fibrinogenului și a fibrinei are ca rezultat polipeptide numite produse de degradare a fibrinei sau produse de fibrină. În starea de homeostază, prezența plasminei este critică, deoarece este o enzimă proteolitică centrală a coagulării și este, de asemenea, necesară pentru degradarea cheagurilor sau fibrinoliză.
În coagularea diseminată intravasculară, procesele de coagulare și fibrinoliză sunt dereglate și rezultatul este coagularea pe scară largă, cu sângerări ulterioare. Indiferent de evenimentul inițial, fiziopatologia afecțiunii este similară în toate condițiile. Unul dintre mediatorii critici este eliberarea unei glicoproteine transmembranare numită factor tisular. Factorul tisular este prezent la suprafața multor tipuri de celule (inclusiv celule endoteliale, macrofage și monocite) și nu este de obicei în contact cu circulația generală, dar este expus circulației după leziuni vasculare. La expunerea la sânge și trombocite, factorul tisular se leagă de factorul VIIa activat (de obicei prezent în urme de sânge), formând complexul tenazic extern. Acest complex activează în continuare factorii IX și X la IXa și respectiv Xa, ducând la o cale comună de coagulare și la formarea ulterioară a trombinei și fibrinei.
Excesul de trombină circulantă rezultă din activarea excesivă a cascadei de coagulare. Excesul de trombină scindează fibrinogenul, care în cele din urmă lasă multe cheaguri de fibrină. Aceste cheaguri în exces captează trombocitele pentru a deveni cheaguri mai mari, ducând la tromboze microvasculare și macrovasculare. Această coagulare în microcirculație, în vasele mari și în organe este ceea ce duce la ischemie, afectarea perfuziei organelor și deteriorarea organelor finale, care apare în sindromul Dick.
În același timp, excesul de trombină circulantă promovează conversia plasminogenului în plasmină, ducând la fibrinoliză. Excesul de plasmină activează, de asemenea, sistemul complementului. Activarea acestor sisteme are ca rezultat multe dintre simptomele clinice pe care le experimentează pacienții cu coagulare intravasculară diseminată, cum ar fi șocul, hipotensiunea și permeabilitatea vasculară crescută. Forma acută a sindromului Dick este considerată a fi o expresie extremă a procesului de coagulare intravasculară cu distrugerea completă a limitelor homeostatice normale.
Cursul clinic al coagulare intravasculară diseminată depinde de motivul apariției sale. Formele acute și severe sunt dominate de manifestări hemoragice - sângerări, ca în complicațiile obstetricale și sepsisul meningococic superacut datorat activării sistemului de coagulare internă de către endotoxine, complexe antigen-anticorp care duc la activarea simultană a sistemului calikrein și a sistemului de dezvoltare a complementului. şoc.
În formele cronice și de grad scăzut, insuficiența multiplă a organelor conduce - cel mai adesea în clinica insuficienței respiratorii acute sau renale acute datorită dominanței coagulării crescute a sângelui.
În coagularea intravasculară diseminată subacută și cronică, complicațiile trombotice apar în prim plan.
Diagnosticul histologic al coagulării intravasculare diseminate se bazează pe trei grupe de caracteristici morfologice:
- semne morfologice directe datorate formării fibrinei - prezența microtrombilor cu structură diferită, tapițeria pereților vaselor cu fibrină, fibrele fibrinei în lumenul vaselor, trombendocardita abacteriană și membranele pulmonare hialine
- semne morfologice ale coagulopatiei de consum - megacariocitemie pulmonară, megacariocite în capilare glomerulare și sinusoide hepatice, hemoragii cu localizare diferită
- semne morfologice tardive - micronecroză diseminată în organe, necroză masivă și infarct, semne morfologice de insuficiență a organelor
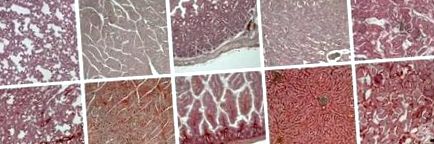
Cel mai semnificativ semn morfologic al coagulării intravasculare diseminate sunt microtrombii multipli localizați în vase cu diametrul mai mic de 200 milimetri (în principal în arteriole, capilare și venule) și mai rar în vase mai mari. Cele mai frecvent afectate de microtrombi sunt plămânii, rinichii, pancreasul, creierul, tractul gastro-intestinal, glandele suprarenale și ficatul.
Macroscopic, în funcție de etapă, putem găsi o imagine patomorfologică diferită, exprimată în general prin semne de hipo- și hipercoagulare - infarcturi multiple de organe, hemoragii multiple pe piele, mucoase și seroase, precum și în diferite organe interne. Cheagurile postmortem sunt puține sau absente, sângele este lichid.
În funcție de modificările stării de coagulare și de manifestările clinice, există mai multe etape ale sindromului DIC acut:
- stadiul hipercoagulării
- stadiul de hipocoagulare cu sau fără coagulopatie evidentă
- stadiul coagulopatiei hiperactive cu hiperfibrinoliză secundară și insuficiență de organ
Patomorfologia coagulării intravasculare diseminate depinde de severitatea, prevalența și stadiul procesului. În stadiul de hipercoagulare, trombina și fibrina se formează ca urmare a activării coagulării sângelui, microtrombii se răspândesc prin fluxul sanguin către diferite organe și se depun în principal în rinichi, plămâni, ficat și piele. Patoanatomic, predomină firele de fibrină plutitoare, pereții vaselor sunt căptușiți cu fibrină și microtrombi liberi de fibrină. În această fază, numărul de cheaguri de sânge este cel mai mare.
În stadiul de hipocoagulare, formarea trombului epuizează rezerva disponibilă de trombocite și factorii de coagulare a plasmei. În absența recuperării compensatorii (dacă există deja leziuni hepatice), se dezvoltă o tulburare de coagulare cu o clinică ușoară de sângerare cu traume minime. Descoperirea patoanatomică arată că în această etapă numărul trombilor scade. Majoritatea sunt fibrină densă sau au formă de globule. Microtrombii mixți și eritrocitari sunt semnificativ mai puțin frecvente. În tromboliza precoce severă (hiperfibrinoliză secundară) sau în stadiile tardive ale sindromului, pot exista doar câțiva microtrombi sau deloc.
Chiar și în această etapă, pot fi observate semnele coagulopatiei consumive, deoarece primul și important semn este apariția unui număr crescut de megacariocite circulante în sângele periferic. Această cicatrice este valabilă în absența bolilor de sânge care să ducă la astfel de modificări. Megacariocitemia se datorează creșterii excreției măduvei osoase a megacariocitelor ca răspuns compensator la creșterea pierderii de trombocite. Mai puțin frecvent, megacariocitele unice pot fi găsite în capilarele glomerulare și sinusoidele hepatice.
În curs subacut sau cronic coagulare intravasculară diseminată dezvoltă trombendocardită abacteriană a valvei mitrale și/sau aortice, cu caracteristica verucoasă sau polipoză, dar fără ulcerație a pliantelor valvulare. Straturile trombotice sunt compuse în principal din trombocite și fibrină. De multe ori devine o sursă de emboli pentru creier.
În stadiul de coagulopatie hiperactivă, se observă semne indirecte tardive ale sindromului, care sunt rezultatul obstrucției trombotice masive care duce la ischemie. În a treia etapă apare hiperfibrinoliza secundară. Din punct de vedere anatomopatologic, există o gamă largă de leziuni, care reprezintă baza morfologică a insuficienței organelor și a mai multor organe - de la micronecroza diseminată la necroza masivă și infarctul în diferite organe interne.
- Plase și inele esofagiene Patologie
- Boala de reflux gastroesofagian Patologie
- Patologie Glossit
- Diverticulul patologiei esofagului
- Glicoproteine Patologie