Dr. Vera Karamfilova, prof. Dr. Zdravko Kamenov
Clinica de endocrinologie și boli metabolice, Spitalul Universitar „Alexandrovska”, MU-Sofia
Sindromul cardiorenal cuprinde un spectru de tulburări care implică inima și rinichii, în care disfuncția acută sau cronică într-un organ poate provoca disfuncție acută sau cronică în celălalt. Include legături încrucișate hemodinamice între rinichi în insuficiența cardiacă și invers, inima în insuficiența renală, precum și tulburări ale unui număr de markeri neurohormonali și căi inflamatorii caracteristice diferitelor fenotipuri. Sindromul metabolic cardiorenal este o formă specifică a sindromului cardiorenal care constă dintr-un complex de tulburări cardiace, renale și metabolice, incluzând rezistența la insulină, obezitate, dislipidemie, hipertensiune arterială și dovezi ale unei boli cardiace și renale precoce. Coexistența insuficienței renale și cardiace la același pacient este asociată cu un prognostic extrem de slab, deoarece mecanismele fiziopatologice și cauza exactă a deteriorării, care stau la baza inițierii și menținerii interacțiunii, sunt complexe, multifactoriale și insuficient studiate.
Cuvinte cheie: sindrom metabolic cardiorenal, diabet zaharat, nefropatie diabetică, insuficiență cardiacă
Sindromul cardiorenal (CRD) a fost descris încă din 1836 de Robert Bright și acoperă o serie de tulburări care implică inima și rinichii, în care disfuncția acută sau cronică într-un organ poate provoca disfuncție acută sau cronică în celălalt organ [1]. De atunci, s-au obținut rezultate semnificative în înțelegerea relației cardiorenale atât în ceea ce privește fenotipurile hemodinamice și fiziopatologia, cât și în ceea ce privește opțiunile terapeutice și rezultatele clinice. Clasificarea actuală a CRC datează din 2008, când Inițiativa pentru Calitatea Dializei Acute a fenotipat CRC în două grupe principale, sindroame cardiorenale și renocardice, pe baza sursei principale a procesului de boală [2]. Divizarea ulterioară include cinci subtipuri în funcție de procesul patogenetic principal și de implicarea secvențială a diferitelor organe (Tabelul 1).
Tabelul 1: Clasificarea CRC de la Conferința de consens privind inițiativa privind calitatea acută a dializei
CCR - sindrom renocardic; CH - insuficiență cardiacă; OSN - insuficiență cardiacă acută; ERC - boală renală cronică; BN - insuficiență renală; ERC - insuficiență renală cronică; ACS - sindrom coronarian acut; OBU - insuficiență renală acută; LVH - hipertrofie ventriculară stângă.
Fenotip
Nume
Descriere
Condiții clinice
CH, ducând la OBN
ACS cu șoc cardiogen și OBU, OSN cu dezvoltarea OBU
Insuficiență cardiacă cronică care duce la BCR
Insuficiență renală acută care duce la OSN
IC în OBU din încărcarea volumului, inflamație și tulburări metabolice în uremie
CKD care duce la IC cronică
LVH și CH din cardiomiopatia asociată cu HBB
Procese sistemice cu dezvoltarea HF și BN
Amiloidoză, sepsis, ciroză
Scopul acestei clasificări consensuale a CRC este de a clarifica caracteristicile diferitelor variante incluse în dereglarea cardiorenală pentru a face un diagnostic mai precis și pentru a aplica tratamentul corect în consecință. Suprapunerea bolilor cardiovasculare și renale are loc prin diferite mecanisme, care includ interacțiuni hemodinamice în insuficiența cardiacă, impactul bolii aterosclerotice în ambele sisteme de organe, activarea neurohormonală, implicarea unui număr de citokine și dezvoltarea modificărilor structurale în inimă. sunt unice pentru progresia bolii renale [3] .
Se știe că inima și rinichii împărtășesc responsabilitatea pentru menținerea stabilității hemodinamice prin controlul comun al ritmului cardiac, al volumului cardiac și al tonusului vascular. Unul dintre mecanismele CRC este asociat cu disfuncția sistolică a ventriculului stâng, care duce la scăderea fluxului sanguin renal, urmată de activarea unui număr de mecanisme de reținere a fluidului și menținerea volumului vascular. Acestea conduc în continuare la deteriorarea capacității cardiace și la reducerea funcției de pompare a inimii odată cu dezvoltarea insuficienței cardiace [4]. Fiziopatologia disfuncției renale în contextul bolilor de inimă este mult mai complexă decât scăderea pur hemodinamică a debitului cardiac, implicând supraactivitate simpatică, sistemul renină-angiotensină-aldosteron (RAAS), diverși mediatori biochimici, prostaglandine (oxizi de azoten) etc. .) precum și stresul oxidativ [5] .
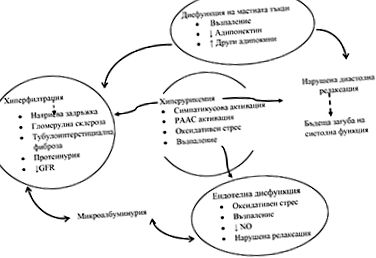
Sindromul metabolic cardiorenal (CRMS) este o formă specifică de CRC care constă dintr-un complex de tulburări cardiace, renale și metabolice, inclusiv rezistența la insulină, obezitate, dislipidemie, hipertensiune arterială, microalbuminurie și dovezi ale bolilor cardiace precoce și ale bolilor renale. 1) [6] .
Figura 1: Mecanisme fiziopatologice ale sindromului metabolic cardiorenal (Modificat de Connell, 2014)
Sindrom metabolic cardiorenal
- Obezitate centrală.
- Rezistenta la insulina.
- Hipertensiune.
- Dislipidemie.
- Proteinurie și/sau funcție renală scăzută.
Obezitatea este o problemă globală de sănătate care afectează milioane de oameni din întreaga lume și este principala cauză a mai multor boli, inclusiv diabetul și bolile cardiovasculare, cel mai frecvent factor fiind rezistența la insulină. Există o legătură puternică între rezistența la insulină și insuficiența cardiacă. Principalii factori care contribuie la dezvoltarea rezistenței la insulină generale și miocardice sunt stresul oxidativ, hiperglicemia, dislipidemia, secreția afectată a adipokinelor și citokinelor, activarea anormală a RAAS și a sistemului nervos simpatic [7]. .
Rezistența la insulină cardiacă apare ca unul dintre factorii principali în dezvoltarea insuficienței cardiace și devine din ce în ce mai importantă datorită creșterii epidemiei atât a obezității, cât și a diabetului. În plus față de mecanismele clasice de rezistență la insulină sistemică, sunt implicați factori suplimentari la nivel miocardic, inclusiv semnalizarea afectată a calciului, alterarea metabolismului substratului, disfuncția mitocondrială, stresul reticulului endoplasmatic, afectarea interacțiunilor endoteliale miocardice și vasculare. Studiile clinice au arătat că riscul evenimentelor cardiovasculare crește de două până la patru ori la pacienții cu DM2, bolile cardiovasculare fiind principala cauză de deces și reprezentând aproximativ 50% din toate decesele cauzate de diabet [9]. .
Pe de altă parte, nefropatia diabetică (DN) este una dintre principalele complicații ale diabetului și o cauză principală a insuficienței renale cronice în stadiul final. Mai mult de 30% dintre pacienții cu diabet dezvoltă DN la 10-20 de ani de la debutul bolii, care este asociat cu o creștere cu 10-30% a costurilor tratamentului [10]. DN se caracterizează printr-o creștere a matricei mezenterice, îngroșarea membranelor bazale glomerulare și tubulare, care în cele din urmă progresează spre glomeruloscleroză și fibroză tubulo-interstițială.
Hiperglicemia persistentă contribuie la aceste procese prin activarea unui număr de căi vasoactive și hormonale, inclusiv RAAS, endotelină, protein kinază - și MAP-kinază, factori de transcripție precum NF-B și alții, ducând la modificări în expresia genică a unui număr de creștere factori și citokine [citokine]. 10]. Din punct de vedere clinic, DN se manifestă prin hipertensiune arterială, proteinurie și funcție renală afectată.
Microalbuminuria este o complicație obișnuită a diabetului și este considerată un predictor puternic al dezvoltării ulterioare a DN. În plus, este asociat cu un risc crescut de evenimente cardiovasculare și mortalitate. Studiile arată că pacienții cu diabet și microalbuminurie sau proteinurie au o progresie de 2-10 ori mai rapidă a bolilor coronariene, a bolilor vasculare și a aterosclerozei [11]. .
Principiile generale ale comportamentului terapeutic în CRC se bazează pe mecanismele fiziopatologice de bază responsabile de menținerea și exacerbarea tulburărilor structurale și funcționale în insuficiența cardiacă și renală, inclusiv inflamația, oxidul nitric și echilibrul radicalilor liberi, sistemul suprarenal simpatic și RAAS. Principalele grupuri de medicamente utilizate sunt diuretice, blocante ale receptorilor angiotensinei (inhibitori ai ECA), blocante ale receptorilor angiotensinei-2 (ARB), blocante directe ale reninei, antagoniști ai calciului, beta-blocante și medicamente inotrope.
Tratamentul medicamentos al CRMS și al diabetului zaharat 2
La pacienții cu DM2, insuficiență cardiacă și DN, a fost propus un nou accent de tratament în contextul sindromului metabolic cardiorenal, cu scopul de a aplica o abordare cuprinzătoare și individuală prin optimizarea terapiei pentru DM2, insuficiență cardiacă și îmbunătățirea funcției renale.
Metformina este un medicament extrem de eficient, cu o istorie lungă în tratamentul DM2, cu beneficii dovedite, cum ar fi un risc scăzut de hipoglicemie, nu provoacă creșterea în greutate și poate reduce evenimentele cardiovasculare și mortalitatea. Este recomandată ca terapie de primă linie pentru majoritatea pacienților cu DM2, pe lângă schimbarea activă a stilului de viață [13]. Cu toate acestea, o proporție mare de pacienți nu reușește să obțină un control adecvat numai cu metformina, necesitând adesea adăugarea unui al doilea și al treilea medicament. Având în vedere impactul controlului glicemic asupra sistemului cardiovascular, în 2008, Administrația SUA pentru Alimente și Medicamente (FDA) a subliniat necesitatea unor studii aprofundate de siguranță cardiovasculară pentru noi medicamente în tratamentul diabetului zaharat [14]. .
Ulterior, mai multe studii de amploare au raportat date impresionante de siguranță cardiovasculară asupra diferitelor clase de medicamente antidiabetice, inclusiv agoniști ai receptorilor peptidului-1 de tip glucagon (GLP-1-RA) și inhibitori ai co-transportorului de sodiu-glucoză-2 (SGLT-2). care a schimbat strategia terapeutică a DM2 [15,16]. La pacienții cu diabet zaharat, cu boli cardiovasculare aterosclerotice stabilite sau cu indicatori de risc crescut, boli renale stabilite sau insuficiență cardiacă, se recomandă tratamentul cu un inhibitor SGLT-2 sau agonist al receptorului GLP-1, cu beneficii dovedite în bolile cardiovasculare, indiferent de nivelul din HbA1c [12]. Alegerea medicamentului este determinată în principal de boala cardiovasculară și/sau renală concomitentă. La pacienții cu insuficiență cardiacă și boli renale cronice, inhibitorii SGLT-2 sunt medicamentul ales, iar în caz de imposibilitate de utilizare a acestora - agonistul receptorului GLP-1 cu efect renoprotector dovedit.
În concluzie, există o legătură puternică între sindromul metabolic cardiorenal și DM2, care se află în centrul obezității și rezistenței la insulină. Fiziopatologia eterogenă și complexă a CRMS, precum și asocierea dintre insuficiența cardiacă și renală la pacienții cu DM2, reprezintă o provocare serioasă în abordările terapeutice moderne. Strategia principală ar trebui să vizeze atât prevenirea obezității, cât și AD2, care este crucială în eforturile de reducere a răspândirii CRM.
- Diabetul - cum să trăiești cu el
- Diabetul și sarcina - cum este dezvăluit
- Diabet - sfaturi și trucuri Doppelherz Bulgaria
- Diabet zaharat și cancer
- Diabet zaharat în timpul sarcinii ICD O24