Dr. A. Yordanov 1, Dr. V. Varbanova 2, Dr. A. Petkov 3, Prof. Dr. Yu. Raynov 2
1 Clinica de hematologie, Spitalul Universitar „St. Ivan Rilski ”, Sofia; 2 Clinica de hematologie, Academia Medicală Militară, Sofia; 3 Cardiologie, Spitalul Universitar „St. Ivan Rilski ”, Sofia
Trombocitemia esențială (ET) este o neoplazie cronică mieloproliferativă, Philadelphia-negativă, care afectează în principal trombocitopoieza cu o frecvență de 0,6-2,5/100.000 populație pe an. Afectarea femeilor cu o incidență maximă de 30-40 de ani și 50-60 de ani predomină [1] .
Caracteristica patognomică a bolii este trombocitoza în sângele periferic (trombocite> 450x109/l), ca urmare a proliferării megacariocitelor mari, mature în măduva osoasă, apoptoza suprimată și tabloul clinic al trombozei și/sau hemoragiei. La fel ca alte tumori maligne, etiologia ET este necunoscută.
Nicio asociere cu expunerea la radiații ionizante sau substanțe chimice, medicamente sau agenți virali.
Cel mai caracteristic semn al ET este trombocitoza din sângele periferic, pe fondul supraviețuirii păstrate a trombocitelor datorită producției crescute a liniei megacariocitare extinse în măduva osoasă.
Motivul acestei creșteri nu este pe deplin înțeles, dar sunt posibile mecanisme complexe, incl. producție autonomă, sensibilitate crescută la citokine (de exemplu, IL-3), efecte scăzute ale factorilor de inhibare a trombocitelor (de exemplu, TGF-β), defecte în micro-mediu.
Majoritatea pacienților cu ET (86%) prezintă mutații în una dintre următoarele trei gene: janus kinaza 2 (JAK2), calreticlin (calreticlin, CALR) sau oncogenă a virusului leucemiei mieloproliferative (MPL) [2] .
Cel mai adesea ET este asociat cu o mutație somatică JAK2 V617F a genei JAK2, care se găsește în 63% din cazuri.
Probabil mutația JAK2 are ca rezultat activarea permanentă a receptorului trombopoietinei, rezultând supraproducția megacariocitelor. Purtătorii mutației JAK2 V617F sunt asociați cu un risc crescut de tromboză arterială și un risc mai mic de MF post-ET. Pacienții au o vârstă medie mai mare, un număr mai mare de hemoglobină și leucocite și un număr relativ scăzut de trombocite [3,4]. .
La 4% din ET, poate apărea o mutație care afectează gena receptorului trombopoietinei (MPL), ceea ce duce la activarea constitutivă a proteinei receptorului trombopoietinei și la proliferarea megacariocitelor. Trombocite mai vechi, mai înalte, mai multe tromboze și risc crescut de transformare - cel mai prost prognostic.
Mutațiile genei CALR apar la 19% dintre pacienții cu ET. Mutația CALR este asociată cu vârsta mai mică, sexul masculin, numărul mai mare de trombocite, nivelul scăzut al hemoglobinei, numărul scăzut al leucocitelor, rata mai scăzută a complicațiilor trombotice. Spre deosebire de pacienții cu mutații JAK2, la care riscul cumulativ de transformare în policitemie este de aproximativ 29% în 15 ani, pacienții cu mutații CALR nu se transformă [4,5]. .
Mutațiile CALR se exclud reciproc cu mutațiile JAK2 sau MPL. La restul de 14% dintre pacienții cu ET, nu a fost detectată nicio mutație „conducătoare” descrisă [2]. .
Tablou clinic
Majoritatea pacienților sunt asimptomatici la începutul bolii. Diagnosticul se face prin examinare aleatorie, care relevă un număr crescut de trombocite. Cea mai frecventă manifestare a bolii și adesea motivul diagnosticului sunt tulburările hemostazei - evenimente hemoragice și trombotice. Pe măsură ce boala progresează și în absența tratamentului, 30-37% dintre pacienți dezvoltă complicații hemoragice, iar 22-84% - trombotice.
La unii pacienți, simptomele inițiale pot fi hepatomegalie și/sau splenomegalie.
Conform clasificării revizuite a tumorilor de țesut hematopoietic și limfoid al Organizației Mondiale a Sănătății (OMS, 2016), diagnosticul ET este acceptat în prezența tuturor celor 4 criterii majore sau a prezenței a 3 criterii majore și minore (Tabelul 1) [1] .
Tabelul 1: Criteriile de diagnostic ale OMS [1]
Criterii grozave
Numărul de trombocite ≥450x109/l.
Biopsia măduvei osoase cu proliferare megacariocitară cu un număr crescut de megacariocite mari, mature, cu nuclei hiperlobulari. Nu există o creștere semnificativă a eritrocitopoiezei și granulocitopoiezei, precum și a ungerii, și foarte rar o ușoară creștere a fibrelor de reticulină (gradul 1).
Criteriile pentru acceptarea următoarelor diagnostice nu sunt îndeplinite: PV, PMF, LMC, MDS, alte neoplazii mieloide.
Prezența mutației JAK2, CALR sau MPL.
Criterii mici
Prezența unui alt marker clonal sau lipsa dovezilor de trombocitoză reactivă.
Evaluarea prognosticului și cursul clinic
Prezența a patru factori independenți asociați cu un risc crescut de complicații tromboembolice împarte pacienții în grupuri de risc cu strategii terapeutice diferite (Tabelul 2) [6,7] .
Tabelul 2: Stratificarea riscului de complicații tromboembolice/hemoragice asociate cu ET
Scara de prognostic ELN
Sau antecedente de complicații tromboembolice sau hemoragice grave asociate cu ET
sau număr de trombocite> 1500x109/l.
Scala prognostică IPSET
Vârsta ≥60 ani - 1 punct.
Antecedente de tromboză sau sângerări majore - 2 t.
Factori de risc SSS - 1 punct.
Mutația JAK2 V617F - 2 t.
Risc foarte mic (0 puncte)
Risc intermediar (2 puncte)
Tabelul 3: Diferențe semnificative statistic în incidența evenimentelor adverse de medicament cu hidroxicarbamidă și anagrelidă [9]
Scopul principal al tratamentului la pacienții cu ET este prevenirea evenimentelor trombotice și hemoragice și controlul simptomelor.
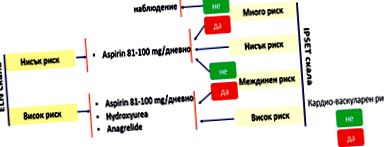
Comportamentul și tratamentul la fiecare pacient sunt determinate după o evaluare atentă a grupului de risc din care face parte (Fig. 1).
Figura 1: Strategia terapeutică în ET [8]
Îmbunătățirea stilului de viață și controlul factorilor de risc concomitenti, precum și utilizarea antiplachetelor trombocitare:
- Renuntarea la fumat.
- Evitarea AINS (medicamente antiinflamatoare nesteroidiene).
- Evitarea tratamentului hormonal (la femei).
Aspirina 75-100 mg/zi.
Se recomandă ca toți pacienții să ia doze profilactic mici de aspirină (cu excepția celor care au contraindicații la aspirină). Studiile arată un risc redus de evenimente trombotice fără a crește incidența evenimentelor hemoragice.
Tratament specific citoreductiv
La un pacient cu risc crescut, pe lângă terapia antiplachetară cu aspirină, o metodă majoră de reducere a riscului de complicații tromboembolice este utilizarea terapiei citoreductive pentru menținerea numărului de trombocite în intervalul de referință.
Hidroxicarbamidă în doză de 0,5-1,5 g/zi. La pacienții cu insuficiență renală, doza trebuie redusă datorită excreției renale a medicamentului.
Anagrelidă - indicat la pacienții cu număr de trombocite în creștere rapidă și rezistență sau intoleranță la hidroxicarbamidă la o doză inițială de 0,5 mg/zi. și titrarea treptată la doza terapeutică obișnuită de 2-3 mg/zi, împărțită în două doze. Rezistența sau intoleranța la tratamentul cu hidroxicarbamidă este luată în considerare în următoarele cazuri:
- Nivel de trombocite> 600 x109/l după 3 luni de tratament în doză de 2 g pe zi.
- Număr de trombocite> 400x109/l combinat cu leucocite [9] .
Interferon-α sau interferon-α pegilat
Mijloace de alegere la pacienții tineri; 3-5x106 UI/zi, de 3-5 ori pe săptămână.
ET are o evoluție lentă și se poate transforma relativ rar într-un alt MPN - în principal mielofibroză (2-5%) sau leucemie acută (5-10%). Speranța de viață este comparabilă cu cea a populației sănătoase din acea vârstă, dar este exacerbată de tromboză fatală sau hemoragie, precum și de efectele secundare ale terapiei. La unii pacienți, tromboza venoasă hepatică duce la hipertensiune portală cu encefalopatie hepatică și rețea colaterală venoasă (varice esofagiene), agravând prognosticul. Scopul principal al terapiei la pacienții cu ET este reducerea riscului de complicații tromboembolice/hemoragice, care sunt cauza supraviețuirii scurtate la 20% dintre pacienții din acest grup, în funcție de caracteristicile individuale ale pacientului și de toxicitatea așteptată a medicamentului [ 8,10] .
- Abordare complexă modernă în sterilitate și endometrioză recurentă - Petar Teodosiev -
- După tratament - Pagina 6
- Abordări moderne în patogeneza, diagnosticul, monitorizarea și tratamentul diabetului gestațional
- Hemoroizii la câini cauzele, simptomele, diagnosticul și caracteristicile tratamentului - Animale de companie - 2021
- Abordări actuale și orientări viitoare în tratamentul recăderii la pacienții cu scleroză multiplă