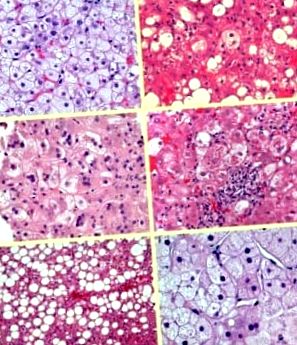
Bolile cumulative sunt unități ale bolii congenitale care se datorează unui defect ereditar sau absenței complete a unei enzime specifice (citoplasmatice sau lizozomale) care este implicată în metabolismul normal. Cele mai frecvente enzime defecte sunt de origine lizozomală, deci acest grup de boli este cunoscut și sub numele de boli lizozomale. Lipsa unei enzime specifice duce la întreruperea lanțului metabolic, cu acumularea ulterioară în celule și țesuturi a unor substanțe intermediare incomplet degradate și insolubile. Acestea perturbă activitatea vitală normală a celulei. Astfel de acumulări anormale de metaboliți sunt observate în celulele diferitelor organe sau sunt fagocitate în mod activ de celulele sistemului monocit-macrofag din splină, ganglioni limfatici și măduva osoasă. Acestea sunt boli care apar în principal în copilărie.
În funcție de tipul de produs metabolic care se acumulează în celule, există:
- glicogenoză
- mucopolizaharidoză
- lipidoză
- asociată cu o tulburare a metabolismului aminoacizilor și nucleoproteinelor
De asemenea, se observă amestecate boli cumulative, în care se acumulează mai multe produse metabolice (mucolipidoză).
Fiecare dintre aceste grupuri mari include boli diferite, în funcție de defectul enzimei specifice. Majoritatea sunt foarte rare. Bolile cumulative sunt ereditare și se transmit în principal prin tip autosomal recesiv. În funcție de gradul defectului sau de absența completă a enzimei, variantele aceleiași boli diferă. În absența completă a unei enzime, se dezvoltă forma infantilă a bolii. În cazurile de conservare a activității enzimatice până la 10-20%, se dezvoltă forma juvenilă. Apoi, atunci când conservarea este în intervalul 70-80%, boala se dezvoltă la adulți.
În multe dintre ele, diagnosticul morfologic pe tot parcursul vieții este posibil cu ajutorul unei biopsii a rectului, a pielii, a ganglionilor limfatici, a organelor interne, a mușchiului scheletic, a măduvei osoase. Acumularea de intermediari insolubili crește dimensiunea celulelor care le conțin. Citoplasma lor devine palidă sau optic goală. Prin urmare, prezența celulelor cu o „celulă de acumulare” caracteristică similară este de o mare importanță pentru diagnostic - „tezaur”.
Examinarea microscopică electronică este, de asemenea, extrem de importantă, ceea ce face posibilă determinarea exactă a localizării substanței anormale sub forma anumitor structuri. De exemplu, substratul microscopic electronic caracteristic al lipidelor este prezentat ca structuri stratificate de tip membrană.
Decisiv pentru diagnostic, care determină tipul de boală cumulativă, rămâne stabilirea defectului enzimatic și tipul substanței depuse prin metode biochimice. Determinarea defectului enzimatic la pacienți și purtători este posibilă în culturile celulare de fibroblaste cutanate. În perioada prenatală, un astfel de studiu este posibil prin analiza lichidului amniotic obținut prin amniocenteză sau cultură celulară din celule amniotice.
Glicogenoză cumulativă este o boală autozomală recesivă. Au o moștenire lipsă de enzime care descompun sau sintetizează glicogenul. Ca urmare, cantități excesive de glicogen normal sau analogii săi anormali se acumulează în diferite organe.
Glicogenul este o polizaharidă foarte ramificată compusă din reziduuri de glucoză. Glicogenul este conținut în citoplasma celulelor sub formă de granule. Granulele conțin, de asemenea, enzimele glicogenogenezei și glicogenolizei. Cele mai mari depozite de glicogen se găsesc în ficat și mușchi. În glicogenogeneză, glicogen sintetazele leagă reziduurile de glucoză prin legături α-1,4-glicozidice în partea neramificată a moleculei. Ramurile sunt formate din legături α-1,6-glicozidice sub acțiunea transglicozidazei amilo-1,4: 1,6. În glicogenoliză, enzimele fosforilază (ficat și mușchi) atacă legăturile α-1,4-glicozidice și rup secvențial lanțul polizaharidic. Legăturile α-1,6-glicozidice situate la punctele de ramificare sunt degradate de E-amilo-1,6-glicozidază.
În plus față de lanțurile metabolice descrise, glicogenul este, de asemenea, degradat în lizozomi de către E-α-1,4-glicozidază (maltază acidă). Dacă este absentă, se dezvoltă singura boală lizozomală după glicogenoză (glicogenoză tip II). Sunt cunoscute 12 tipuri de glicogenoză. Unele dintre ele sunt extrem de rare. La fiecare dintre ele s-a constatat lipsa unei enzime. În funcție de lipsa unui ficat, mușchi sau enzimă specific localizat în multe organe, există diferite forme de glicogenoză hepatică, musculară sau generalizată.
În glicogeneza de tip I, nu s-au observat rezultate specifice în ficat, dar au fost detectate cantități mai mari de glicogen normal, precum și infiltrare grasă. Poate exista o tulburare a hepatocitelor datorată depunerii de glicogen și lipide. Fibroza hepatică și ciroză nu apar. Constatările histologice la rinichi includ scleroza glomerulară focală, fibroza interstițială, atrofia sau vacuolarea tumorii și ateroscleroza semnificativă. Se produce hipertrofie glomerulară proeminentă și, mai rar, apar depozite lipidice multiple în mezangiul glomerular, celulele epiteliale tubulare și interstitiu. Microscopia electronică poate dezvălui îngroșarea difuză a membranei glomerulare și a picăturilor lipidice din mezangiu.
În glicogeneza de tip II, analiza ultrastructurală a unui număr mare de probe diferite de țesut relevă cantități mari de glicogen normal. Într-o biopsie musculară la microscop cu lumină și colorare cu hematoxilină și eozină, se poate identifica un „model de dantelă”. Cu colorare periodică cu Acid-Schiff, fibrele musculare sunt puternic colorate în forma pediatrică. La microscopul electronic, biopsiile musculare prezintă miopatie vacuolară cu stocare a glicogenului în lizozomi și glicogen liber în citoplasmă, dar eșecul identificării acestei descoperiri nu poate exclude un diagnostic.
Tabloul histologic al ficatului la pacienții cu glicogenoză de tip III se caracterizează prin dizolvarea totală a celulelor hepatice din glicogen și țesut fibros. Procesul fibrotic poate fi caracterizat prin boală periportală minimă sau ciroză micronodulară. Acest lucru nu este de obicei progresiv.
În glicogeneza de tip IV, biopsia hepatică și musculară a prezentat hepatocite PAS-pozitive mărite și incluziuni rezistente la diastază. Histocitele spumante din sistemul reticuloendotelial pot fi observate și în ficat. Fibroza interstițială este, de asemenea, prezentă, se observă agregate fibrilare de material asemănător amilopectinei la microscopul electronic.
În glicogeneza de tip V, descoperirile histologice sunt nespecifice. În glicogenotipul VI, hepatocitele dilatate de glicogenul acumulat (adică particule alfa, formă de rozetă) pot fi observate în ficat și sunt mai puțin compacte decât în glicogenozele clasice de tip I și III. În glicoza de tip VII, polizaharida anormală se acumulează cu morfologia fibrilară în mușchiul scheletic.
Mucopolizaharidoza este un grup de tulburări metabolice cauzate de absența sau funcționarea defectuoasă a enzimelor lizozomale necesare pentru descompunerea moleculelor numite glicozaminoglicanii. Aceste lanțuri lungi de glucide din zahăr se găsesc în celule care ajută la construirea oaselor, cartilajului, tendoanelor, corneei, pielii și țesutului conjunctiv. Glucosaminoglicanii (denumiți anterior mucopolizaharide) se găsesc și în fluidele care lubrifiază articulațiile.
Pacienții cu mucopolizaharidoză fie nu produc suficient din cele unsprezece enzime necesare pentru descompunerea acestor lanțuri de zahăr în molecule mai simple, fie produc enzime care nu funcționează corect. În timp, acești glicozaminoglicanii se acumulează în celule, sânge și țesut conjunctiv. Rezultatul este afectarea permanentă, progresivă a celulelor care afectează aspectul, abilitățile fizice, funcționarea organelor și a sistemului și, în majoritatea cazurilor, dezvoltarea mentală.
Mucopolizaharidoza face parte din familia de stocare lizozomală, un grup de peste 40 de tulburări genetice care apar atunci când un organul lizozomal din celule este deteriorat. Lizozomul poate fi considerat un centru de reciclare a celulei, deoarece procesează materialul nedorit în alte substanțe pe care celula le poate folosi. Lizozomii descompun această materie nedorită prin enzime, proteine foarte specializate, care sunt esențiale pentru supraviețuire. Tulburările lizozomale, cum ar fi mucopolizaharidoza, sunt declanșate atunci când există o enzimă în prea mică sau complet absentă.
Sunt cunoscute șapte tipuri clinice diferite și mai multe subtipuri de mucopolizaharidoză. Deși fiecare mucopolizaharidoză este clinic diferită, majoritatea pacienților au de obicei o perioadă de dezvoltare normală urmată de o scădere a funcției fizice și/sau mentale.
În toate tipurile de mucopolizaharidoză, pielea normală sau ușor îngroșată prezintă granule metacromatice în fibroblaste utilizând colorarea Giemsa sau albastru de toluidină. Aceste granule metacromatice sunt aparente ocazional în keratinocite și în structurile eccrine. Furnicăturile caracteristice ale pielii în sindromul Hunter prezintă aceste granule în fibroblastele dermice și materialul metacromatic extracelular între fasciculele de colagen. În toate tipurile de mucopolizaharidoză, citoplasma limfocitelor circulante prezintă și aceste granule. Pacienții cu sindrom Morquio prezintă activitate redusă de N-acetil-galactozamină-6-sulfatază pe cultura fibroblastelor obținută dintr-o probă de biopsie a pielii.
O altă boală a stocării lizozomale, adesea confundată cu mucopolizaharidoză, este mucolipidoza. În această boală, în plus față de zaharuri, sunt stocate cantități excesive de substanțe grase cunoscute sub numele de lipide (o altă componentă majoră a celulelor vii). Persoanele cu mucolipidoză pot împărtăși unele dintre semnele clinice asociate cu mucopolizaharidoză (anumite caracteristici faciale, tulburări osoase și leziuni cerebrale), iar nivelurile crescute de enzime necesare pentru descompunerea lipidelor se găsesc în sânge.
Lipidele cumulative sunt cel mai mare grup boli cumulative. Sunt boli determinate genetic, cu moștenire autozomală recesivă a unui defect enzimatic lizozomal specific. Ca urmare, intermediarii nedegrași ai lipidelor complexe se acumulează în diferite organe.
Lipidoza cumulativă apare clinic cu afectarea severă a sistemului nervos central, motiv pentru care se mai numește și neurolipidoză. Dintre neurolipidoze, cel mai mare grup este swingolipidoză. În funcție de tipul de tulburare a metabolismului lipidic, swingolipidoza este împărțită în gangliozidoză, cerebrozidoză, sulfatidoză și swingomielinoză.
- Care sunt simptomele bolilor de inimă
- Patologia clinică a calculilor renali Patologie
- Patologia clinică a aspergilozei Patologie
- Caz clinic Alcoolism cronic și boli hepatice Știri medicale
- Patologia clinică a nefritei lupusului Patologie