Edemul pulmonar este o acumulare de lichid în țesuturile și spațiile aeriene ale plămânilor. Acest lucru duce la alterarea schimbului de gaze și poate provoca insuficiență respiratorie. Acest lucru se datorează fie eșecului ventriculului stâng în eliminarea adecvată a sângelui din circulația pulmonară (edem pulmonar cardiogen), fie deteriorării parenchimului pulmonar sau a vasculaturii pulmonare (edem pulmonar non-cardiogen).
Etiologie
Edemul pulmonar este o afecțiune clinică și patologică generală. Tulburările hemodinamice sau modificările permeabilității microvasculare pot provoca edem pulmonar. Când se depășește capacitatea sistemului limfatic de drenare a lichidului interstițial, se dezvoltă edem interstițial. Când există o creștere suplimentară a presiunii interstițiale, conexiunile strânse dintre celulele epiteliale alveolare se deschid și fluidul se deplasează în spațiile alveolare, provocând edem alveolar. Edemul cronic predispune la infecție.
Scurgerea fluidului este determinată de diferența dintre presiunea hidrostatică capilară și presiunea hidrostatică intermediară, presiunea hidrostatică fiind mai mare. Resorbția fluidelor este determinată de diferența de presiune oncotică dintre cele două compartimente. Cantitatea de fluid emis este modulată de caracteristicile de permeabilitate ale membranei capilare alveolare.
În funcție de factorii cauzali, edemul pulmonar este hemodinamic și permeabil.
Edemul pulmonar hemodinamic apare ca urmare a unei creșteri accentuate a presiunii hidrostatice în microcirculația pulmonară. Se datorează insuficienței cardiace stângi acute, cel mai frecvent în infarctul miocardic, miocardită și defecte cardiace. Geneza edemului neurogen vasomotor datorită vasoconstricției reflexe a venulelor pulmonare este similară. Edemul pulmonar cu un mecanism patogenetic similar se poate dezvolta și în leziunile cerebrale traumatice și în tumorile cerebrale care duc la creșterea presiunii intracraniene.
Permeabilitatea edem pulmonar din cauza:
- tulburări microcirculatorii severe care duc la creșterea permeabilității vasculare, cum ar fi șocul și procesele inflamatorii în plămâni
- leziuni alveolare difuze de la diverse substanțe toxice
Leziunea pulmonară poate provoca, de asemenea, edem pulmonar prin vătămarea vasculaturii și parenchimului pulmonar. Sindromul de detresă respiratorie acută acoperă multe dintre aceste cauze, dar acestea pot include:
- inhalarea gazelor fierbinți sau toxice
- leziuni pulmonare, adică traume de mare energie (accidente auto)
- aspirație, de exemplu, lichid gastric
- re-expansiune, adică toracenteză cu volum mare, rezoluția pneumotoraxului, postcorticație, îndepărtarea obstrucției endobronșice, formă eficientă de edem pulmonar cu presiune negativă.
- leziuni de reperfuzie, adică tromboendartectomie postpulmonară sau transplant pulmonar
- edem pulmonar indus de înot, cunoscut și sub numele de edem pulmonar prin imersie
- supraîncărcarea circulatorie legată de transfuzie apare atunci când sângele sau produsele din sânge (plasmă, trombocite) sunt transfuzate în mod repetat pentru o perioadă scurtă de timp.
- transfuzia asociată cu leziuni pulmonare acute este un tip specific de leziune prin transfuzie de sânge care apare atunci când plasma donatoare conține anticorpi împotriva destinatarului, cum ar fi anticorpi anti-HLA sau anti-neutrofili.
- infecție sau inflamație severă, care poate fi locală sau sistemică
Tablou clinic
Cel mai frecvent simptom al edemului pulmonar este dificultatea respirației, dar poate include alte simptome precum hemoptizia (denumită în mod clasic spută roz, spumoasă), transpirație excesivă, neliniște și piele palidă. Scăderea respirației se poate prezenta ca ortopnee și/sau dispnee nocturnă paroxistică (episoade de scurtare bruscă severă pe timp de noapte). Acestea sunt simptome frecvente ale edemului pulmonar cronic datorat insuficienței ventriculare stângi. Dezvoltarea edemului pulmonar poate fi asociată cu simptome și semne de „supraîncărcare lichidă”. Acesta este un termen nespecific pentru a descrie manifestările insuficienței ventriculare drepte în restul corpului și include edem periferic, presiune venoasă jugulară crescută și hepatomegalie, în care ficatul este mărit și poate fi fraged sau chiar pulsant. Alte semne includ respirația șuierătoare la expirare, auscultarea și prezența unui al treilea tonus cardiac.
Pacienții cu edem pulmonar cardiogen au caracteristicile clinice dramatice ale insuficienței cardiace stângi. Pacienții dezvoltă un debut brusc de dificultăți de respirație, anxietate și senzație de înec. Cel mai adesea se plâng de dificultăți de respirație și diaforeză abundentă. Pacienții cu simptome progresive (peste 24 de ore) raportează adesea dificultăți de respirație, ortopnee și dispnee nocturnă paroxistică.
Tusea este o problemă frecventă și poate oferi o indicație timpurie a agravării edemului pulmonar la pacienții cu disfuncție cronică a ventriculului stâng. Sputa roz, spumoasă poate fi prezentă la pacienții cu boli severe. Ocazional, răgușeala poate fi prezentă ca urmare a comprimării paraliziei recurente a nervului laringian prin atriul stâng dilatat, de exemplu în stenoza mitrală (semnul lui Ortner).
Durerea toracică ar trebui să alerteze medicul cu privire la posibilitatea unei ischemii acute/infarctului miocardic sau a unei disecții aortice cu insuficiență aortică acută ca precipitat al edemului pulmonar.
Patogenie
Patogeneza hidrostaticului edem pulmonar se atribuie în primul rând unei diferențe în forțele Starling (adică, extracția fluidelor datorată unui gradient crescut de presiune hidrostatică sau scăzut de presiune oncotică peste bariera alveolar-capilară intactă). În plus, capacitatea sistemului limfatic de a elimina fluidul din spațiul interstițial și de a se scurge în venele sistemice depinde de presiunea venoasă sistemică și de integritatea sistemului limfatic. Tabloul clinic al afecțiunii este dominat de congestia pulmonară datorată creșterii acute după efort. Creșterea postîncărcării poate fi principalul mecanism responsabil de edemul pulmonar care cauzează disfuncție cardiacă acută și congestie pulmonară sau poate fi secundară unei disfuncții cardiace majore.
Într-un studiu recent, mecanismul a fost descris ca o consecință a unei creșteri accentuate a încărcăturii post-pacient la pacienții cu capacitate sistolică și diastolică redusă de a se adapta la modificările de sarcină în prezența funcției de sprijin ventricular drept. Ipoteza este că pacienții cu edem pulmonar răspund la creșterea postîncărcării cu ritm cardiac crescut și vasoconstricție periferică, mai degrabă decât cu adaptare acută la dimensiunea inimii. Acest lucru sugerează că există dimensiuni mai mici ale inimii și ritm cardiac mai mare și tensiune arterială diastolică în comparație cu alte profiluri.
Deși mecanismele legate de presiune sunt considerate suficiente pentru a explica boala, studii recente au arătat că edemul pulmonar cardiogen este reglementat critic de procesele de semnalizare activă, sugerând că răspunsurile endoteliale și alveolare pot contribui în mod critic la edemul pulmonar hidrostatic. Absorbția lichidului alveolar în exces este un proces activ care implică transportul de sodiu din spațiile aeriene alveolare cu apă după gradientul osmotic de sodiu. Transportul activ de sodiu transeptal de la spațiul aerian la spațiul interstițial pulmonar este un mecanism major care guvernează clearance-ul fluidului alveolar. Acest mecanism depinde de absorbția de sodiu de către canalele de sodiu sensibile la amilorură de pe membrana apicală a celulelor alveolare de tip II, urmată de extrudarea de sodiu pe suprafața basolaterală de adenozin trifosfatază sodică-potasică.
O parte majoră a formării edemului pulmonar cardiogen este rezultatul secreției epiteliale active de clor și a fluxului secundar de lichid în spațiul alveolar. Secreția de clor transepitelial este activată prin inhibarea absorbției de sodiu epitelial și mediată de un regulator al conducerii transmibrale a fibrozei chistice și a co-transportorului de sodiu-clorură de potasiu 1.
Transportul activ de sodiu prin epiteliul alveolar este, de asemenea, reglementat de sodiu-potasiu-adenozin trifosfatază bazolaterală, iar o creștere bruscă a presiunii atriale inhibă transportul activ de sodiu prin scăderea numărului de sodiu-potasiu-adenozin trifosfat alfa din bază. Reglarea sa este indusă de stimularea receptorilor dopaminergici, beta-2 adrenergici și a aldosteronului și este inhibată de compuși asemănători cu oabain. În plus, datele recente sugerează că leziunile pulmonare și disfuncția barierei pot juca un rol în formarea și rezolvarea congestiei și a edemului pulmonar.
Caracteristici patologice
Inițial, edemul pulmonar interstițial apare cu dilatarea septurilor interalveolare și vacuolarea celulelor endoteliale. Începe din zonele adiacente și se extinde treptat periferic. Ulterior, edemul pneumocitelor și scurgerea edemului în cavitățile alveolare - edem alveolar.
În edemul pulmonar hemodinamic, lichidul edematos are un conținut scăzut de proteine și transudat. Dimpotrivă, în edemul de permeabilitate este bogat în proteine și atunci când este amestecat cu aerul în alveole prezintă tendința de a forma spumă și, uneori, la niveluri ridicate de fibrinogen și activitate fibrinolitică suprimată și membrane pulmonare hialine.
Macroscopic, plămânii sunt măriți, grei și cărnoși. Suprafața lor tăiată este suculentă și din ea curge mult lichid.
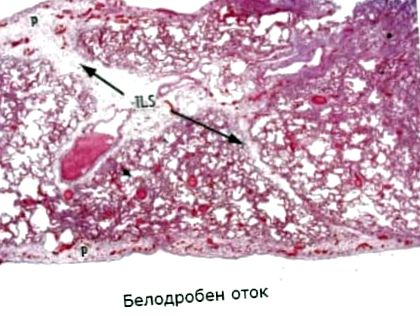
Microscopic, septurile alveolare sunt dilatate, iar alveolele sunt umplute cu un lichid colorat cu eozină roz pal, fără aproape celule. Cu edem permeabil în fluidul edematos se pot observa multe bule mici de aer - plămâni „spumoase”. Cu edem pulmonar prelungit, poate apărea creșterea țesutului conjunctiv pericapilar.
Cu o mărire mare, alveolele din plămân prezentate în figura 1 sunt umplute cu un material roz neted până la ușor flocular caracteristic edemului pulmonar. Capilarele din pereții alveolari sunt supraîncărcate cu multe celule roșii din sânge. Obstrucția și umflarea plămânilor sunt frecvente la pacienții cu insuficiență cardiacă și în zonele cu pneumonie.
Edemul pulmonar cu capilare dilatate și fluxul de sânge către spațiile alveolare are ca rezultat o creștere a macrofagelor hemosiderinei, așa cum se arată în Figura 2. Granulele brune de hemosiderină din defalcarea globulelor roșii apar în citoplasma macrofagelor. Aceste macrofage sunt uneori denumite „celule ale insuficienței cardiace” datorită asocierii lor cu insuficiența cardiacă congestivă.
- Edem pulmonar
- Edem pulmonar
- Edemul pulmonar - poate fi fatal
- Pulmonar - Asociați de cardiologie capitală
- Adenocarcinomul intestinului subțire Patologie