Colita ulcerativă este o boală inflamatorie difuză, nespecifică a colonului și rectului a cărei etiologie este necunoscută. Mucoasa colonului, proximală a rectului, este afectată permanent, implicând adesea eroziuni și/sau ulcere, precum și cicluri recurente de recurență și remisie și potențiale manifestări extraintestinale.
Principalele simptome ale bolii active sunt durerile abdominale și diareea amestecate cu sânge. Pot apărea și pierderea în greutate, febră și anemie. Adesea simptomele apar încet și pot varia de la ușoare la severe. Simptomele apar de obicei periodic, cu perioade în care nu există simptome.
Colita ulcerativă este mai frecventă la caucazieni decât la negri sau latino. Se raportează că frecvența sa este de 2-4 ori mai mare în rândul evreilor askenazi. Boala este puțin mai frecventă la femei decât la bărbați. Vârsta de debut urmează un model bimodal, cu un vârf la 15-25 de ani și mai mic la 55-65 de ani, deși boala poate apărea la persoanele de orice vârstă. Colita ulcerativă este rară la persoanele cu vârsta sub 10 ani. Doi din 100.000 de copii sunt afectați. Cu toate acestea, 20% -25% din toate cazurile de colită ulcerativă apar la persoane cu vârsta de cel puțin 20 de ani.
În prezent se ia în considerare cauza colitei ulcerative. Deși nu a fost elucidată nicio cauză specifică, multe etiologii au fost postulate și studiate. Se crede că boala se dezvoltă secundar după interacțiuni complexe între predispozițiile genetice, factorii de risc de mediu și sistemul imunitar. Mai multe gene joacă probabil un rol. Produsele lor, în combinație cu factorii de mediu și imunitatea disfuncțională, conduc la un spectru al bolii cu manifestări eterogene și fenotipuri foarte unice.
O teorie sugerează că colita ulcerativă apare ca rezultat direct al unui răspuns imun anormal la „antigenul luminal intestinal” la o gazdă sensibilă genetic. În mucoasa colonică a pacienților normali, celulele fagocitare nu răspund la bacteriile locale. La pacienții cu boli inflamatorii intestinale, aceste fagocite pot începe să răspundă la flora intestinală prin secretarea de citokine pro-inflamatorii care activează o populație specifică de celule T. Acest lucru duce la inflamație și deteriorarea căptușelii. În special, se speculează că interleukina-25, care controlează unele aspecte ale răspunsului celulelor T-helper, poate fi anormală sau deficitară la unii pacienți cu boală inflamatorie intestinală.
Trebuie remarcat faptul că flora microbiotică la pacienții cu boală inflamatorie intestinală este mai puțin diversă decât la persoanele neafectate: indivizii sănătoși au mai multe comensale intestinale („bacterii bune”), în timp ce cei cu boli inflamatorii intestinale au mai mulți agenți patogeni intestinali („bacterii rele” ). Deși unii agenți patogeni, inclusiv Pectinatus, Sutterella și Fusobacterium, sunt frecvente în colita ulcerativă, nu a fost demonstrată nicio asociere patogenetică cu colita ulcerativă.
O altă ipoteză este că anticorpii se formează împotriva anumitor bacterii și produse bacteriene din intestin și că acești anticorpi propagă răspunsul imun modificat prezent în bolile inflamatorii intestinale. Pe scurt, cercetările anterioare și literatura de specialitate au arătat că, atunci când predispoziția genetică este combinată cu anumiți factori de mediu - atât externi, cât și interni - și afectată de un răspuns imun modificat, pot apărea boli inflamatorii intestinale. Nu au fost identificate modificări dietetice sau de mediu care ar putea preveni boala inflamatorie a intestinului sau îmbunătăți definitiv evoluția bolii.
Colita ulcerativă poate implica difuz întregul colon sau poate fi limitată la rect (proctită ulcerativă).
În clasic colită ulcerativă proba de rezecție totală arată de obicei un proces continuu de schimbare, începând cu rectul și progresând proximal, terminând peste tot în colon până la valva ileocecală. Mucoasa poate fi hiperemică și nodulară și poate prezenta o granularitate fină (Figura 1). Pot apărea eroziuni și ulcere. Ulcerele sunt de obicei largi și pot fi liniare sau geografice. Ulcerele sunt de obicei superficiale, dar uneori pot implica straturi mai profunde. Fundul lor este necrotic, iar marginile sunt sfâșiate. Sângele, puroiul sau mucusul pot acoperi mucoasa. Formarea pseudopolipilor este foarte specifică pentru colita ulcerativă.
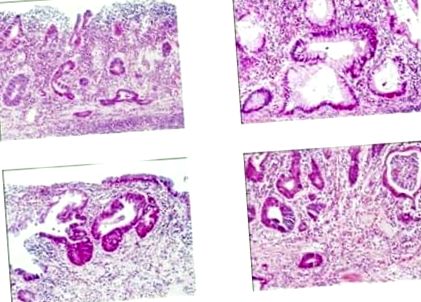
Microscopic, afecțiunea se caracterizează prin congestie vasculară și edem, infiltrat inflamator, care include leucocite eozinofile și neutrofile, abcese de criptă (Figura 2). Există puțină infiltrare inflamatorie în submucoasă sau nu există modificări vizibile. Pe suprafața mucoasei există mucus, fibrină și epiteliu exfoliat.
În anumite zone mucoasa este necrotică, iar ulcerarea părților necrotice prezintă defecte ulcerative. Acoperă stratul mucoasei și rareori pătrund mai adânc. Țesutul de granulație poate fi găsit la baza defectului ulcerului. În alte ulcere, țesutul de granulație umple defectul, uneori chiar ieșind deasupra acestuia, ca un polip.
Ca urmare a proceselor regenerative intensificate, mucoasa conservată în jurul ulcerelor poate fi hipertrofiată. Există glande mărite abundent, cu secreție slabă de mucus în epiteliu, care iese deasupra nivelului mucoasei. Stratul muscular al peretelui intestinal este hipertrofiat și umflat. Dacă ating defectele ulcerative, apare un infiltrat inflamator în aceste zone.
În faza de atenuare a procesului, se observă ulcere granulare, pseudopolipi regenerativi și cicatrizarea defectelor ulcerative, dar fără epitelizare completă.
Pacienții cu colită ulcerativă sunt expuși riscului de displazie, care crește odată cu durata bolii, precum și o probabilitate crescută de adenocarcinom în comparație cu grupurile de vârstă fără boală inflamatorie intestinală. Recunoașterea histologică a displaziei și a carcinomului este crucială.
Displazia este definită ca o modificare neoplazică neechivocă a epiteliului colonului. Poate consta în dezorganizarea arhitecturală a criptelor colonului, atipii citologice (inclusiv hipercromasia nucleară), pseudostratificare, pleomorfism, cromatină condensată și foi nucleare proeminente, cu activitate mitotică crescută, în special în partea superioară a criptelor (Figura 3).
În displazia de grad scăzut, nucleii ar trebui să fie limitați la o mare parte a jumătății bazale cu asemănare citologică cu adenoamele tubulare ale colonului, diferă de displazia de grad înalt într-o mare măsură, cu diferențe de atipicitate citologică.
În displazia de grad înalt, stratificarea nucleară se extinde la aspectul superior (luminal) al celulelor și există o pierdere a polarității nucleare, inclusiv pierderea orientării axei lungi a nucleului de la perpendicular la membrană, care poate varia de la celulă la celulă, însoțit de rotunjiri nucleare.
Categoriile acceptate includ displazia nedeterminată, displazia de grad scăzut și displazia de grad înalt. Poate fi dificil să se distingă displazia de atipia reactivă/reparativă care apare după perioade de activitate a bolii. Aceste diagnostice trebuie făcute cu prudență, deoarece consecințele pentru pacient sunt grave.
În perioadele de odihnă la colită ulcerativă se poate vedea o căptușeală complet invizibilă a colonului. Alternativ, poate fi evaluată o reducere generală a numărului de cripte, distanța inegală și alte modificări arhitecturale cronice. Poate exista fibroză în lamina propria, mucoasa musculară îngroșată și metaplazia Panet.
- Colită ulcerativă (HUHK)
- Examen histologic Patologie
- Diateza hemoragică Patologie
- Dieta pentru colita BG-Mamma
- Patologia colecistitei cronice